
 A、B、C、D、E进行焰色反应均显黄色,这些物质能实现如图所示的转化关系.其中A为淡黄色固体,C为强碱.
A、B、C、D、E进行焰色反应均显黄色,这些物质能实现如图所示的转化关系.其中A为淡黄色固体,C为强碱.分析 A、B、C、D、E进行焰色反应均显黄色,则都含有Na元素,A为淡黄色固体,应为Na2O2,C为强碱,应为NaOH,由转化关系可知D为Na2CO3,B为Na,E为NaCl,以此解答该题.
解答 解:A、B、C、D、E进行焰色反应均显黄色,则都含有Na元素,A为淡黄色固体,应为Na2O2,C为强碱,应为NaOH,由转化关系可知D为Na2CO3,B为Na,E为NaCl,
(1)B为Na,性质活泼,实验室一般保存在煤油中,故答案为:保存在煤油中;
(2)A为Na2O2,与二氧化碳反应生成碳酸钠,方程式为2Na2O2+2CO2=2Na2CO3+O2↑,B为Na,与水反应生成氢氧化钠,方程式为2Na+2H2O=2NaOH+H2↑,
故答案为:2Na2O2+2CO2=2Na2CO3+O2↑;2Na+2H2O=2NaOH+H2↑;
(3)焰色反应为物理变化,进行焰色反应使用的主要仪器为铂丝,先将铂丝放在酒精灯的火焰上灼烧,直至与火焰原来的颜色相同,然后蘸取待测液,放在火焰上灼烧,观察颜色,每次试验完都要用盐酸洗净铂丝,在火焰上灼烧至与火焰原来的颜色相同为止,
故答案为:物理;先将铂丝放在酒精灯的火焰上灼烧,直至与火焰原来的颜色相同,然后蘸取待测液,放在火焰上灼烧,观察颜色.
点评 本题考查无机物推断,涉及钠元素化合物性质及相互转化,“A为淡黄色固体,C为强碱”是推断的突破口,再结合转化关系进行推断,难度中等.


 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 三聚氰胺的摩尔质量为126g/mol | |
| B. | 三聚氰胺分子中各元素原子的物质的量之比为n(C):n(H):n(N)=1:2:2 | |
| C. | 三聚氰胺分子中各元素的质量比为m(C):m(H):m(N)=6:1:14 | |
| D. | 标准状况下,1mol三聚氰胺所占的体积约为22.4 L |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
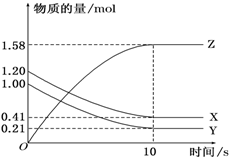 一定温度下,某1L体积固定的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示,请回答下列问题:
一定温度下,某1L体积固定的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示,请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含有NA个二氧化碳分子 | B. | 含有1molO2 | ||
| C. | 质量为44 g•mol-1 | D. | 所占的体积为22.4L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 乙醇 | 溴乙烷 | 1-丁醇 | 1-溴丁烷 | |
| 密度/g•cm-3 | 0.7893 | 1.4604 | 0.8098 | 1.2758 |
| 沸点/℃ | 78.5 | 38.4 | 117.2 | 101.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com