
某无色溶液中只可能含有Na+、Ba2+、Cl-、Br-、SO32-、SO42-离子中的若干种,依次进行下列实验,且每步所加试剂均过量,观察到的现象如下:

下列结论正确的是
A.肯定含有离子的Na+、Br-、SO32- B.肯定没有的离子是Ba2+、SO32-
C.可能含有的离子是Cl-、Br-、SO42- D.不能确定的离子是Na+、Cl-、SO42-
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2014-2015山东省枣庄市高一上学期期末化学试卷(解析版) 题型:选择题
固体X只可能由Al、(NH4)2SO4、MgCl2、FeCl2、AlCl3中的一种或几种组成,某同学对该固体进行了如下实验

下列判断正确的是:
A.气体甲一定是纯净物
B.白色沉淀乙不一定是Al(OH)3
C.固体X中一定存在 (NH4)2SO4、 MgCl2
D.固体X中一定存在FeCl2、AlCl3
查看答案和解析>>
科目:高中化学 来源:2014-2015江西省新余市高一上学期期末考试化学试卷(解析版) 题型:选择题
下列叙述中正确的是
A.硫酸的摩尔质量是98g
B.铁原子的摩尔质量等于铁的相对原子质量
C.标准状况下,22.4L的O2质量是32g
D.2g H2所含原子物质的量为1mol
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省遂宁市高三第二次诊断考试化学试卷(解析版) 题型:选择题
已知浓度商(Qc)表示任意状态下反应体系中物质的浓度关系,其表达式与化学平衡常数的表达式相同。保持温度和体积不变,可逆反应:A(s) + 2B(g) 2C(g) + D(g) △H<0, 在甲、乙、丙三个容器中建立平衡的相关信息如下表。则下列说法正确的是
2C(g) + D(g) △H<0, 在甲、乙、丙三个容器中建立平衡的相关信息如下表。则下列说法正确的是
容器 | 体积 | 起始物质 | 平衡时C的 物质的量 | 平衡时B的 体积分数 | 平衡常数 |
甲 | 1L | 1molA+2molB | 1mol | φ甲 | K甲 |
乙 | 1L | 4molC+2molD | n1 mol | φ乙 | K乙 |
丙 | 2L | 4molC+2molD | n2 mol | φ丙 | K丙 |
A.在建立平衡的过程中,甲的Qc逐渐减小,乙和丙的Qc逐渐增大
B.K甲=K丙>K乙
C.升高甲的温度,可使φ甲=φ乙
D.n1=1.6,n2=2
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省日照市高三3月模拟考试理综化学试卷(解析版) 题型:推断题
(12分)【化学一有机化学基础】
聚乙酸乙烯酯又名聚醋酸乙烯酯,主要用作涂料、胶黏剂、纸张、口香糖基料和织物整理剂,其合成路线如下,其中物质J与氯化铁溶液能发生显色反应。
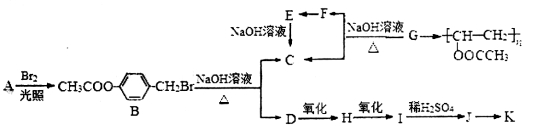
已知:①当羟基与双键碳原相连时,易发生如下转化RCH=CHOH→RCH2CHO;
②—ONa连在烃基上不易被氧化。
请回答下列问题:
(1)写出G的结构简式__________;F与H中具有相同官能团的名称___________。
(2)J在一定条件下能生成高聚物K,K的结构简式是___________________。
(3)同时符合下列要求的A的同分异构体有_____________种。
①含有苯环
②苯环上有2个取代基
③能发生银镜反应和水解反应
(4)写出B→C+D反应的化学方程式:______________________________________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省日照市高三3月模拟考试理综化学试卷(解析版) 题型:选择题
化学与能源开发、环境保护、生产生活等密切相关。下列叙述错误的是
A.光催化水制氢比电解水制氢更节能环保
B.用聚乙烯塑料代替聚乳酸塑料可减少白色污染
C.开发利用可再生能源,可减少化石燃料的使用
D.改进汽车尾气净化技术,可减少大气污染物的排放
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖南省怀化市高三第一次模拟考试理综化学试卷(解析版) 题型:选择题
下列叙述正确的是
A.常温下,10 mL 0.02 mol·L-1 HCl溶液与10 mL 0.02 mol·L-1 Ba(OH)2溶液充分混合,若混合后溶液的体积为20 mL,则溶液的pH=12
B.常温下,向AgCl的饱和溶液中加入NaCl固体,有固体析出,且AgCl的Ksp变小
C.在0.1 mol·L-1 CH3COONa溶液中,c(OH-)>c(CH3COOH)+c(H+)
D.常温下pH=4的NaHC2O4溶液中:c(H2C2O4)>c(C2O42-)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省泉州五校高三上学期摸底联考化学试卷(解析版) 题型:选择题
100mL浓度为2mol·L-1的盐酸溶液跟过量的锌片反应,为减慢反应速率,又不影响生成H2的总量,可采用的方法有
A.加适量6mol·L-1HCl溶液
B.加数滴CuCl2溶液
C.加适量醋酸钠固体
D.加适量NaNO3溶液
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市石景山区高三上学期期末考试化学试卷(解析版) 题型:实验题
(10分)电子工业中,可用FeCl3—HCl溶液作为印刷电路铜板蚀刻液。某探究小组设计如下线路处理废液和资源回收:
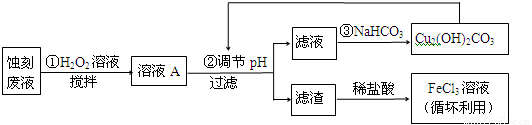
请回答:
(1)FeCl3—HCl溶液蚀刻铜板后的废液中含有的金属阳离子是 。
(2)FeCl3蚀刻液中加入盐酸的目的:可以 ,又可提高蚀刻速率。
(3)步骤①中加入H2O2溶液的目的是 。
(4)已知:生成氢氧化物沉淀的pH
Cu(OH)2 | Fe(OH)2 | Fe(OH)3 | |
开始沉淀时 | 4.7 | 7.0 | 1.9 |
沉淀完全时 | 6.7 | 9.0 | 3.2 |
根据表中数据推测调节pH的范围是 。
(5)写出步骤②中生成CO2的一个离子方程式_____(已知Cu2(OH)2CO3不易溶于水)。
(6)写出步骤③生成Cu2(OH)2CO3的离子方程式___________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com