
 W��X��Y��Z�����ֳ����Ķ�����Ԫ�أ���ԭ�Ӱ뾶��ԭ�������仯��ͼ��ʾ����֪W��һ�ֺ��ص�������Ϊ18��������Ϊ10��X��Neԭ�ӵĺ�����������1��Y�ĵ�����һ�ֳ����ġ��뵼����ϣ�Zԭ�ӵõ���������ͬ��������Ԫ�������ģ�
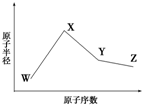
W��X��Y��Z�����ֳ����Ķ�����Ԫ�أ���ԭ�Ӱ뾶��ԭ�������仯��ͼ��ʾ����֪W��һ�ֺ��ص�������Ϊ18��������Ϊ10��X��Neԭ�ӵĺ�����������1��Y�ĵ�����һ�ֳ����ġ��뵼����ϣ�Zԭ�ӵõ���������ͬ��������Ԫ�������ģ����� W��X��Y��Z�����ֳ����Ķ�����Ԫ�أ�W��һ�ֺ��ص�������Ϊ18��������Ϊ10������������Ϊ18-10=8����WΪOԪ�أ�X��Neԭ�ӵĺ�����������1����ԭ�Ӱ뾶������������XΪNaԪ�أ�Y�ĵ�����һ�ֳ����İ뵼����ϣ�ԭ����������Na����YΪSi��Z�ĵõ���������ͬ��������Ԫ�������ģ���ZΪ�ڢ���A��Ԫ�أ�ԭ����������Si������ZΪClԪ�أ��ݴ˽��
��� �⣺W��X��Y��Z�����ֳ����Ķ�����Ԫ�أ�W��һ�ֺ��ص�������Ϊ18��������Ϊ10������������Ϊ18-10=8����WΪOԪ�أ�X��Neԭ�ӵĺ�����������1����ԭ�Ӱ뾶������������XΪNaԪ�أ�Y�ĵ�����һ�ֳ����İ뵼����ϣ�ԭ����������Na����YΪSi��Z�ĵõ���������ͬ��������Ԫ�������ģ���ZΪ�ڢ���A��Ԫ�أ�ԭ����������Si������ZΪClԪ�أ�
��1��XΪNaԪ�أ�λ��Ԫ�����ڱ��е������ڵ�IA�壻W��Ԫ�ط���ΪO��
�ʴ�Ϊ������IA��O��
��2��X����Ϊ�ƣ����ڽ������壬���۵�Ƚϵͣ�Y�ĵ���Ϊ�裬����ԭ�Ӿ��壬�е����Na�����ڷǽ�����Cl��Br�����⻯���ȶ���HCl��HBr��
�ʴ�Ϊ��Si��HCl��
��3��Y��Z�γɵĻ�����ΪSiCl4����������ˮ��Ӧ������һ�������һ��ǿ�ᣬӦ�õ�������HCl���÷�Ӧ�Ļ�ѧ����ʽ��SiCl4+3H2O=H2SiO3��+4HCl��
�ʴ�Ϊ��SiCl4+3H2O=H2SiO3��+4HCl��
��4��Y�ǹ�Ԫ�أ����⻯��ΪSiH4����������ȼ�շ�����Ӧ��SiH4+2O2�TSiO2+2H2O��ƽ��ÿת��lmol����ʱ�μӷ�Ӧ��ΪSiH4Ϊ$\frac{1mol}{8}$=0.125mol����1molSiH4��Ӧʱ�ų�������Ϊ190.0kJ��$\frac{1mol}{0.125mol}$=1520kJ��
�ʴ�Ϊ��1520kJ��
���� ���⿼��λ�ýṹ���ʹ�ϵӦ�ã��ƶ�Ԫ���ǽ���ؼ������ضԻ�ѧ������Ԫ�������ɵĿ��飬������ѧ���Ի���֪ʶ�Ĺ��̣��Ѷ��еȣ�


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���� | B�� | ��ȩ | C�� | ���� | D�� | �������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CH3OH | B�� | ��CH3��2CHOH | C�� | ��CH3��3COH | D�� | ��CH3��3CCH2OH |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | HCI��Һ�����Ա�H2S��Һ������ǿ | |
| B�� | ��������������Һ��Ӧ��H2S+C12�T2HCl+S�� | |
| C�� | �Ȼ���������ȶ� | |
| D�� | HClO4�����Ա�H2SO4ǿ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | �٢ڢ� | B�� | �ڢۢ� | C�� | �ܢݢ� | D�� | �ۢܢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | A��B��C��D | B�� | D��A��B=C | C�� | A=B��C=D | D�� | D��A��B��C |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ���� | ��A | ��A | ��A | ��A | ��A | ��A | ��A | O�� |
| 1 | ||||||||
| 2 | G | H | D | |||||
| 3 | B | C | E | |||||
| 4 | F | A |
 ���õ���ʽ��ʾAD2���γɹ���
���õ���ʽ��ʾAD2���γɹ��� ��
�� ��
���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com