
【题目】利用下图装置,可以模拟铁的电化学防护。下列说法正确的是( )

A. 若X为碳棒,为减缓铁的腐蚀,开关K应该置于M处
B. 若X为锌,开关K置于M处,该电化学防护法称为牺牲阳极的阴极保护法
C. 若X为碳棒,K与M连接时,一段时间后溶液的pH减小
D. 若X为锌,K与N连接时,X电极产生气泡
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】某反应中反应物与生成物有FeCl2、FeCl3、CuCl2、Cu。
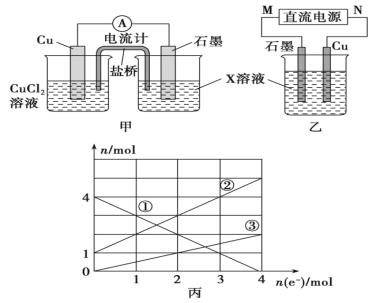
(1)将上述反应设计成的原电池如图甲所示,请回答下列问题:
①图中X溶液是____(填化学式);
②Cu电极上发生的电极反应式为________;
③原电池工作时,电子通过电流计的方向是____(填“从左到右”或“从右到左”);盐桥中的____(填“K+”或“Cl-”)不断进入X溶液中。
(2)将上述反应设计成的电解池如图乙所示,乙烧杯中金属阳离子的物质的量与电子转移的物质的量的变化关系如图丙,请回答下列问题:
①M是____极;
②图丙中的②线是____(填离子)的变化。
③当电子转移为2mol时,向乙烧杯中加入____L 5 mol·L-1NaOH溶液才能使所有的金属阳离子沉淀完全。
(3)铁的重要化合物高铁酸钠(Na2FeO4)是一种新型饮用水消毒剂,具有很多优点。
①高铁酸钠的生产方法之一是电解法,其原理为Fe+2NaOH+2H2O![]() Na2FeO4+3H2↑,则电解时阳极的电极反应式是__________。
Na2FeO4+3H2↑,则电解时阳极的电极反应式是__________。
②高铁酸钠的生产方法之二是在强碱性介质中用NaClO氧化Fe(OH)3生成高铁酸钠、氯化钠和水,该反应的离子方程式为_______。
(4)向10mL1mol·L-1NH4Al(SO4)2溶液中滴加1mol·L-1NaOH溶液,沉淀的物质的量随加入NaOH溶液体积的变化如图所示(滴加过程无气体放出)。
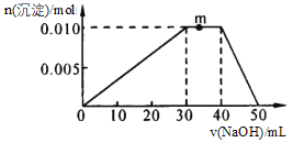
①写出m点发生反应的离子方程式____。
②若在该盐溶液中改加20mL1.2mol·L-1Ba(OH)2溶液,充分反应后,溶液中产生沉淀的物质的量为____________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A的化学式为NH5,它的所有原子的最外层都符合相应的稀有气体原子的最外层电子层结构,则下列有关说法中,正确的是_____
A.1 mol NH5中含有5NA个N—H键(NA表示阿伏加德罗常数)
B.NH5中既有共价键又有离子键,NH5是离子化合物
C.NH5的电子式为![]()
D.它与水反应的化学方程式为NH5+H2O=NH3·H2O+H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科研人员提出了由CO2和CH4转化为高附加值产品CH3COOH的催化反应历程。该历程示意图如下。

下列说法不正确的是
A. 生成CH3COOH总反应的原子利用率为100%
B. CH4→CH3COOH过程中,有C―H键发生断裂
C. ①→②放出能量并形成了C―C键
D. 该催化剂可有效提高反应物的平衡转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】HBr被![]() 氧化依次由如下Ⅰ、Ⅱ、Ⅲ三步反应组成:
氧化依次由如下Ⅰ、Ⅱ、Ⅲ三步反应组成:
Ⅰ.HBr(g)+O2(g)=HOOBr(g);
Ⅱ.HOOBr(g)+HBr(g)=2HOBr(g);
Ⅲ.HOBr(g)+HBr(g)=H2O(g)+Br2(g)
1mol HBr(g)被氧化为![]() (g)放出
(g)放出![]() 热量,其能量与反应进程的关系如图所示:
热量,其能量与反应进程的关系如图所示:
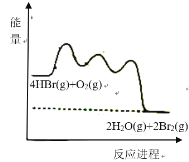
下列说法正确的是![]()
![]()
A.反应Ⅰ、Ⅱ、Ⅲ均为放热反应
B.Ⅰ的反应速率最慢
C.HOOBr比HBr和![]() 稳定
稳定
D.热化学方程式为:4HBr(g)+O2(g)=2H2O(g)+2Br2(g) ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】部分短周期元素原子半径的相对大小、最高正价或最低负价随原子序数的变化关系如图:
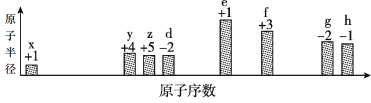
下列说法不正确的是
A.x、z、d三种元素能形成具有强氧化性的酸
B.g、h氧化物对应的水化物都是强酸
C.e最高价氧化物对应的水化物是强碱
D.f的氧化物是两性氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如何降低大气中![]() 的含量及有效地开发利用
的含量及有效地开发利用![]() 引起了全世界的普遍重视。目前工业上有一种方法是用
引起了全世界的普遍重视。目前工业上有一种方法是用![]() 来生产燃料甲醇。为探究该反应原理,进行如下实验:在容积为1L的密闭容器中,充入
来生产燃料甲醇。为探究该反应原理,进行如下实验:在容积为1L的密闭容器中,充入![]() 和
和![]() ,在
,在![]() 下发生发应
下发生发应![]() 实验测得
实验测得![]() 和
和![]() 的物质的量
的物质的量![]() 随时间变化如图1所示:
随时间变化如图1所示:
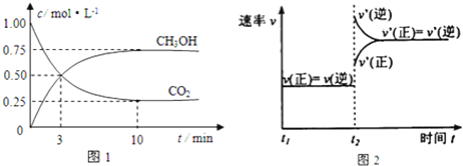
(1)下列事实能说明反应到达平衡状态的是______________
A.容器内的密度不再改变 B. CO2和H2 的物质的量比不再改变
C.v正(CO2)=3v逆(H2) D. 容器内的压强不再改变
(2)![]() 达平衡时,
达平衡时,![]() 的体积分数为____________,平衡常数为______
的体积分数为____________,平衡常数为______![]() 保留两位小数
保留两位小数![]() ;该温度下,测得某时刻,
;该温度下,测得某时刻,![]() 、
、![]() 、
、![]() 和
和![]() 的浓度均
的浓度均![]() ,则此 时
,则此 时![]() 正
正![]() ______
______![]() 逆
逆![]() 填“
填“![]() ”“
”“![]() ”或“
”或“![]() ”
”![]() 。
。
(3)由图2可知,当温度升高到![]() 达平衡时,K值__________
达平衡时,K值__________![]() 填“增大”“减小”或“不变”
填“增大”“减小”或“不变”![]() 。
。
(4)下列措施中不能使![]() 的转化率增大的是______。
的转化率增大的是______。
A.在原容器中再充入1mol![]()
B.在原容器中再充入![]()
C.缩小容器的容积
![]() 使用更有效的催化剂
使用更有效的催化剂
E.将水蒸气从体系中分离出
F.在原容器中充入1molHe
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,水存在如下电离:H2O![]() H++OH- H>0,下列叙述正确的是
H++OH- H>0,下列叙述正确的是
A.向水中滴入少量稀盐酸,平衡逆向移动,Kw减小
B.将水加热,Kw增大,pH减小
C.向水中加入少量固体NH4Cl,平衡逆向移动,c(H+)降低
D.向水中加入少量固体硫酸钠,c(H+)=10-7mol/L,Kw不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,向0.1mol/L醋酸中通入氯化氢气体,下列描述不正确的是( )
A. pH逐渐减小B. c(H+)增大
C. 水的电离程度会不断增大D. Kw不变
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com