
| A�� | X��W��U������������Ӧ��ˮ����������ǿ������˳��Ϊ��U��W��X | |
| B�� | Y��ZԪ�صĵ������缫��������������Һ�й���ԭ��أ�Z�缫�ϲ����������� | |
| C�� | �����£�0.05��mol•L-1U����̬�⻯���ˮ��Һ��pH��1 | |
| D�� | Y��Z��UԪ�صļ����Ӱ뾶�ɴ�С��˳��Y��Z��U |
���� ������Ԫ��X��Y��Z��W��Uԭ��������������Wԭ�ӵ������������Ǵ�����������һ�룬���ԭ��������֪��Wֻ�ܴ��ڵ������ڣ�����������Ϊ4����WΪSi��X��Wλ��ͬһ���壬��XΪCԪ�أ�Y��Z�γɵ���������dz������ͻ���ϣ���YΪMg��ZΪAl��Z��W��Uԭ�ӵ�����������֮��Ϊ13����Uԭ������������Ϊ13-3-4=6����UΪSԪ�أ�
��� �⣺������Ԫ��X��Y��Z��W��Uԭ��������������Wԭ�ӵ������������Ǵ�����������һ�룬���ԭ��������֪��Wֻ�ܴ��ڵ������ڣ�����������Ϊ4����WΪSi��X��Wλ��ͬһ���壬��XΪCԪ�أ�Y��Z�γɵ���������dz������ͻ���ϣ���YΪMg��ZΪAl��Z��W��Uԭ�ӵ�����������֮��Ϊ13����Uԭ������������Ϊ13-3-4=6����UΪSԪ�أ�
A���ǽ�����S��C��Si��������������Ӧ��ˮ����������ǿ������˳��Ϊ�����̼����ᣬ��A����
B��Mg��AlԪ�صĵ������缫��������������Һ�й���ԭ��أ�Al��������������Һ��Ӧ����Mg���ܣ���AlΪ������MgΪ��������Mg�缫�ϵ缫�ϲ���������������B����
C������Ϊ������ʣ�0.05��mol•L-1�����ˮ��Һ��������Ũ��С��0.1mol/L������Һ��pH��1����C��ȷ��
D�����Ӳ�ṹ��ͬ�����ӣ��˵����Խ�����Ӱ뾶ԽС�����ӵ��Ӳ�Խ�����Ӱ뾶Խ�����Ӱ뾶S2-��mg2+��Al3+����D����
��ѡ��C��
���� ���⿼��ṹ����λ�ù�ϵӦ�ã���Ŀ�Ƚ��ۺϣ��漰Ԫ�������ɡ�ԭ���ԭ������ҺpH�����뾶�Ƚϵȣ��ؼ��dz������ԭ��������������������Ų��ص��ƶ�WԪ�أ��Ѷ��еȣ�


 һ����������ϵ�д�
һ����������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��������������ͧ | B�� | �Ȼ���������Ӳˮ������ | ||
| C�� | ʯӢɰ���������������� | D�� | ���ķ���ϩ�����ڳ��߱���Ϳ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
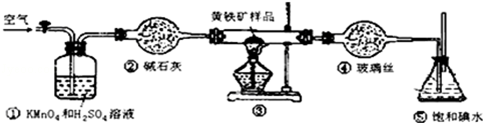
| �ζ����� | ����Һ������/mL | ������Һ�����/mL | |
| �ζ�ǰ | �ζ��� | ||
| ��һ�� | 20.00mL | 0.00 | 20.98 |
| �ڶ��� | 20.00mL | 0.22 | 20.20 |
| ������ | 20.00mL | 0.36 | 20.38 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
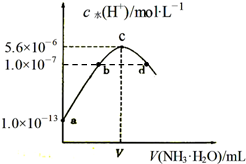 �����£���20mLijŨ�ȵ�������Һ�е���0.1mol•L-1��ˮ����Һ��ˮ�����������Ũ������백ˮ������仯��ͼ�����з�����ȷ���ǣ�������
�����£���20mLijŨ�ȵ�������Һ�е���0.1mol•L-1��ˮ����Һ��ˮ�����������Ũ������백ˮ������仯��ͼ�����з�����ȷ���ǣ�������| A�� | ��ͼ��֪ϡ�����Ũ��Ϊ0.1 mol•L-1 | |
| B�� | b����ҺpH=7 | |
| C�� | c����ʾ��Һ�У�c��SO42-����c��NH4+����c��H+����c��OH-�� | |
| D�� | d����ʾ��Һ�У�c��NH4+��=2c��SO42-�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ԭ��������X��Y��Z��W | |
| B�� | ���Ӱ뾶��W��X��Z | |
| C�� | W�ֱ���Y��Z�γɵĻ������л�ѧ�����Ͳ�ͬ | |
| D�� | ��̬�⻯����ȶ��ԣ�W��Y |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
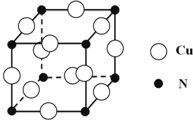 ��͵�Ԫ���ڻ�ѧ���к���Ҫ�ĵ�λ���ش��������⣺
��͵�Ԫ���ڻ�ѧ���к���Ҫ�ĵ�λ���ش��������⣺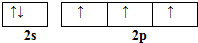 ��Ԥ����2017�귢��ġ��϶���š�̽�������õij���5�����ػ��ȼ��Ϊƫ������[��CH3��2NNH2]����CH3��2NNH2��Nԭ�ӵ��ӻ���ʽΪsp3��
��Ԥ����2017�귢��ġ��϶���š�̽�������õij���5�����ػ��ȼ��Ϊƫ������[��CH3��2NNH2]����CH3��2NNH2��Nԭ�ӵ��ӻ���ʽΪsp3��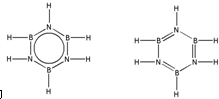 ����
�����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
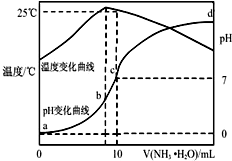 ��ij�¶�ʱ����nmol•L-1��ˮ����10mL1.0mol•L-1�����У���ҺpH���¶�����백ˮ����仯������ͼ��ʾ�������й�˵����ȷ���ǣ�������
��ij�¶�ʱ����nmol•L-1��ˮ����10mL1.0mol•L-1�����У���ҺpH���¶�����백ˮ����仯������ͼ��ʾ�������й�˵����ȷ���ǣ�������| A�� | a��Kw=1.0��10-14 | |
| B�� | 25��ʱNH4Clˮ�ⳣ��Ϊ����n-1����10-7mol•L-1����n��ʾ�� | |
| C�� | b�㣺c��NH4+����c��Cl-����c��H+����c��OH-�� | |
| D�� | ˮ�ĵ���̶ȣ�b��c��a��d |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
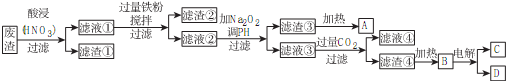
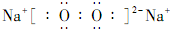 ��
���鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com