
在智利硝石矿层中含有碘酸钠,可用亚硫酸氢钠与其反应来制备单质碘,其化学方程式是:2NaIO3+5NaHSO3=3NaHSO4+2NaSO4+I2+H2O
(1)反应中 元素被氧化, 是氧化剂.
(2)反应产物中,氧化产物与还原产物的物质的量之比为 .
| 氧化还原反应. | |
| 专题: | 氧化还原反应专题. |
| 分析: | 2NaIO3+5NaHSO3=3NaHSO4+2NaSO4+I2+H2O中,I元素的化合价由+5价降低为0,S元素的化合价由+4价升高为+6价,以此来解答. |
| 解答: | 解:(1)S元素的化合价升高,则S元素失去电子被氧化,I元素的化合价降低,则NaIO3为氧化剂,故答案为:S;NaIO3; (2)S元素的化合价升高,含S物质为还原剂被氧化,对应的产物NaHSO4、NaSO4为氧化产物,氧化剂被还原,对应的产物I2为还原产物,则由反应中化学计量数可知氧化产物与还原产物的物质的量之比为(3+2):1=5:1,故答案为:5:1. |
| 点评: | 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应基本概念的考查,注意从化合价角度分析,题目难度不大. |


 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案科目:高中化学 来源: 题型:
按下列要求完成各小题:
(1)Na2O2的电子式 ,该化合物属于 化合物;
(2)H2O分子的结构式;
(3)NH3分子的空间构型是 ;
(4)CO2分子的球棍模型 (注意原子半径的大小);
(5)非金属性最强的元素与原子半径最小的元素形成的化合物的电子式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
金属a、b的活泼性均比氢强,a还可以从b的硝酸盐中置换出b。将a、b用导线相连放入CuSO4溶液,下列叙述中不正确的是( )
A.导线上有电流,电流方向由b向a
B.a极质量减小,b极质量增加
C.b极上放出氢气
D.a极发生氧化反应,b极发生还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
某溶液中只含有Na+、Al3+、Cl﹣、SO42﹣ 四种离子,已知前三种离子的个数比为3:2:1,则溶液中Al3+和 SO42﹣的离子个数比为( )
|
| A. | 1:2 | B. | 1:4 | C. | 3:4 | D. | 3:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
向含有下列离子的溶液中分别加入烧碱固体(溶液体积变化可忽略),能引起离子浓度减小的是( )
|
| A. | CO32﹣ | B. | Cl﹣ | C. | OH﹣ | D. | Cu2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
“奥运会”严格禁止运动员服用兴奋剂.关于某种兴奋剂(结构简式如图)的以下说法中,正确的是( )
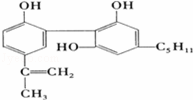
|
| A. | 该物质属于芳香烃 |
|
| B. | 该物质所有原子都在同一平面上 |
|
| C. | 该物质的分子式为C20H25O3 |
|
| D. | 1mol该物质最多能与7mol H2加成 |
查看答案和解析>>
科目:高中化学 来源: 题型:
绿色化学的核心是反应过程的绿色化,要求原料物质中的所有原子完全被利用且全部转入期望的产品中.下列过程不符合这一思想的是( )
|
| A. | 甲烷、CO合成乙酸乙酯:2CH4+2CO |
|
| B. | 烯烃与水煤气发生的羰基合成反应:RCH=CH2+CO+H2 |
|
| C. | 乙醇被氧气催化氧化成乙醛 |
|
| D. | 氯乙烯合成聚氯乙烯 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于热化学反应的描述中正确的是( )
|
| A. | HCl和NaOH反应的中和热△H=﹣57.3kJ/mol,则H2SO4和Ca(OH)2反应的中和热△H=2×(﹣57.3)kJ/mol |
|
| B. | CO(g)的燃烧热是283.0kJ/mol,则2CO2(g)═2CO(g)+O2(g)反应的△H=+566.0kJ/mol |
|
| C. | 需要加热才能发生的反应一定是吸热反应 |
|
| D. | 1mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com