
| A. | 液氨、液氯、干冰、碘化银均为化合物 | |
| B. | 明矾、小苏打、醋酸、次氯酸均为电解质 | |
| C. | 碘酒、牛奶、豆浆、漂白粉均为胶体 | |
| D. | Na2O2、Na2CO3、Na2SiO3、KNO3均为盐 |
分析 A.化合物是不同元素组成的纯净物,液氨是氨气属于化合物、液氯是单质;
B.电解质是水溶液中或熔融状态下导电的化合物;
C.胶体的本质特征是分散质微粒直径在1nm-100nm间;
D.盐是金属阳离子和酸根阴离子构成的化合物.
解答 解:A.液氨为液态氨气,属于纯净的化合物,干冰、碘化银均为化合物,液氯是单质,故A错误;
B.明矾、小苏打、醋酸、次氯酸,符合电解质概念,均为电解质,故B正确;
C.碘酒是碘单质的酒精溶液、牛奶、豆浆是胶体,漂粉粉为次氯酸钙、氯化钙的混合物,故C错误;
D.Na2CO3、Na2SiO3、KNO3均为盐,Na2O2没有酸根离子,所以不是盐,是过氧化物,故D错误;
故选B.
点评 本题考查了化学基本概念的理解和应用,熟悉混合物、化合物、单质、化合物、电解质、非电解质等概念的分析即可判断,掌握物质的组成是解题关键,题目难度不大.


 名题金卷系列答案
名题金卷系列答案科目:高中化学 来源: 题型:选择题
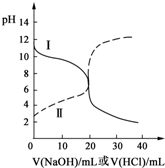 25℃时取浓度均为0.1000mol•L-1的CH3COOH(aq)和氨水各20mL,分别用0.1000mol•L-1NaOH(aq)、0.1000mol•L-1盐酸进行中和滴定,滴定过程中pH随滴加溶液的体积变化关系如图所示.下列说法正确的是( )
25℃时取浓度均为0.1000mol•L-1的CH3COOH(aq)和氨水各20mL,分别用0.1000mol•L-1NaOH(aq)、0.1000mol•L-1盐酸进行中和滴定,滴定过程中pH随滴加溶液的体积变化关系如图所示.下列说法正确的是( )| A. | 曲线Ⅰ:滴加溶液到10.00mL时:c(CH3COO-)>c(Na+)>c(H+)>c(OH-) | |
| B. | 曲线Ⅱ:滴加溶液到10.00mL时:c(CH3COO-)-c(CH3COOH)=2[c(OH-)-c(H+)] | |
| C. | 曲线Ⅱ:滴加溶液在10.00mL~20.00mL之间存在:c(NH4+)=c(Cl-)>c(OH-)=c(H+) | |
| D. | 曲线Ⅰ:滴加溶液到20.00mL时,c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1个 | B. | 2个 | C. | 3个 | D. | 4个 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
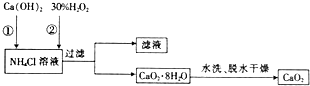
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢气通过灼热的Cu0粉末 | B. | 二氧化碳通过Na202粉末 | ||
| C. | 铝粉与Fe203粉末发生铝热反应 | D. | 将锌粉投入CuSO4溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+、Fe3+、Cl-、SCN- | B. | NH4+、H+、NO3-、SO42- | ||
| C. | Ba2+、Na+、HCO3-、SO42- | D. | Fe2+、K+、MnO4-、OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1,3-环己二烯加氢是吸热反应 | |
| B. | 完全燃烧时1,3-环己二烯比苯放热多 | |
| C. | 苯加氢生成环己烷是吸热反应 | |
| D. | 苯比1,3-环己二烯稳定 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com