
| A. | V(NaOH)=10时,c(OH-)+c(H2C2O4)═c(C2O42-)+c(H+) | |
| B. | V(NaOH)=100 mL时,可能存在c(Na+)>2c(C2O42-)+c(HC2O4-) | |
| C. | V(NaOH)=1000 mL时,c(Na+)>c(HC2O4-)>c(C2O42-)>c(H2C2O4) | |
| D. | V(NaOH)=10 mL时,溶液中c(H+)=1×10-12 mol/L |
分析 A.V(NaOH)=10 mL时,溶液中溶质为Na2C2O4,溶液中存在电荷守恒和物料守恒分析;
B.V(NaOH)=100 mL时,溶液显碱性,结合电荷守恒分析;
C.V(NaOH)=1000 mL时,氢氧化钠大量存在,c(HC2O4-)<c(C2O42-);
D.V(NaOH)=10 mL时,溶液中溶质为Na2C2O4,存在水解平衡:C2O42-+H2O?HC2O4-+OH-,结合定量平衡常数和离子积常数计算分析.
解答 解:A.V(NaOH)=10 mL时,溶液中溶质为Na2C2O4,溶液中存在电荷守恒c(Na+)+c(H+)=2c(C2O42-)+c(HC2O4- )+c(OH-),溶液中物料守恒为:c(Na+)=2c(C2O42-)+2c(HC2O4-)+2c(H2C2O4),得到c(OH-)=2c(H2C2O4)+c(HC2O4- )+c(H+),故A错误;
B.V(NaOH)=100 mL时,溶液显碱性,c(H+)<c(OH-),c(Na+)+c(H+)=2c(C2O42-)+c(HC2O4- )+c(OH-),一定存在c(Na+)>2c(C2O42-)+c(HC2O4-),故B错误;
C.V(NaOH)=1000 mL时,氢氧化钠大量存在,c(HC2O4-)<c(C2O42-),c(Na+)>c(C2O42-)>c(HC2O4-)>c(H2C2O4),故C正确;
D.V(NaOH)=10 mL时,溶液中溶质为Na2C2O4,存在水解平衡:C2O42-+H2O?HC2O4-+OH-,Kh=$\frac{c(O{H}^{-})c(H{C}_{2}{{O}_{4}}^{-})}{c({C}_{2}{{O}_{4}}^{2-})}$=$\frac{c(O{H}^{-})c(H{C}_{2}{{O}_{4}}^{-})}{c({C}_{2}{{O}_{4}}^{2-})}$×$\frac{c({H}^{+})}{c({H}^{+})}$=$\frac{Kw}{K{a}_{2}}$=$\frac{1{0}^{-14}}{6.4×1{0}^{-5}}$=1.56×10-10,故D错误;
故选C.
点评 本题考查溶液中离子的关系,明确溶液中的溶质是解答的关键,并注意利用溶液中水解的程度及电离的程度、电荷守恒来分析解答,题目难度中等.


科目:高中化学 来源:2016-2017学年山东省高二上10月月考化学试卷(解析版) 题型:选择题
根据热化学方程式S(s)+O2(g)===SO2(g) ΔH=-297.23kJ·mol-1,分析下列说法中正确的是
①S(g)+O2(g)===SO2(g) ΔH=-Q,Q值大于297.23kJ·mol-1
②S(g)+O2(g)===SO2(g) ΔH=-Q,Q值小于297.23kJ·mol-1
③1molSO2的键能总和大于1molS与1molO2的键能总和
④1molSO2的键能总和小于1molS与1molO2的键能总和
A.①③ B.②④ C.①④ D.③④
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省成都市高一上10月月考化学试卷(解析版) 题型:选择题
相同状况下,n mol氢气和n mol二氧化碳的体积相同,下列解释比较全面的是:①n mol氢气和n mol二氧化碳所含的气体分子数目相同;②相同状况下,氢分子间的平均距离和二氧化碳分子间的平均距离大致相等;③氢分子本身的大小和二氧化碳分子本身的大小大致相同;④气体分子本身大小相对分子间平均距离来说可忽略不计
A.①②③ B.①②④ C.①④ D.①③
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | AgCl沉淀多于AgBr沉淀 | B. | AgCl和AgBr沉淀等量生成 | ||
| C. | AgCl沉淀少于AgBr沉淀 | D. | 只有AgBr沉淀生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.742吨 | B. | 0.85吨 | C. | 0.875吨 | D. | 1吨 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
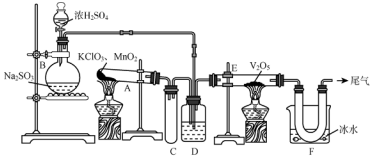
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
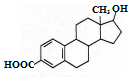
| A. | 该有机物的分子式为C19H22O3 | |
| B. | 该分子中所有碳原子不可能在同一个平面内 | |
| C. | 能发生加成反应、取代反应、水解反应 | |
| D. | 能与Na、NaOH溶液反应,但不能与NaHCO3溶液反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com