
【题目】(1)玻璃棒是化学实验中常用的仪器之一,其主要用于搅拌、过滤或转移液体时的引流。下列实验过程中,通常不需要使用玻璃棒的是___________(填序号,下同)
①用pH试纸测定Na2CO3溶液的pH
②用适量的蔗糖、浓硫酸和水在小烧杯中进行浓硫酸的脱水性实验
③实验室中用FeCl3溶液和沸水制取Fe(OH)3胶体
④用已知浓度的稀盐酸滴定未知浓度的氢氧化钠溶液
⑤取某溶液做焰色反应实验,检验该溶液中是否含有钠元素
(2)①下列仪器在使用前一定要检查是否漏液的是______________________。
a.容量瓶 b.冷凝管 c.碱式滴定管 d.长颈漏斗 e.分液漏斗
②检查装置气密性是化学实验中的重要操作之一。不进行气密性检查可能导致的后果是____________。
a.收集不到气体 b.造成环境污染
c.观察到的实验现象有误 d.引发爆炸事故
(3)下图所示装置可用于制备某种干燥的纯净气体。该装置中所盛装的药品正确的是_____________。
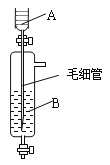
a.A中装浓硫酸,B中装浓盐酸
b.A中装浓盐酸,B中装浓硫酸
c.A中装氢氧化钠浓溶液,B中装浓氨水
d.A中装浓氨水,B中装氢氧化钠浓溶液
【答案】 ③④⑤ ace abcd b
【解析】(1)①用pH试纸测定Na2CO3溶液的pH,可用玻璃棒蘸取溶液;②进行浓硫酸的脱水性实验,应用玻璃棒不断搅拌;③无需使用玻璃棒;④用已知浓度的盐酸和未知浓度的氢氧化钠溶液进行中和滴定实验;⑤做焰色反应实验,用铂丝蘸取待测液;(2)①在高中阶段常见仪器需要检漏的有:分液漏斗、容量瓶、酸式滴定管和碱式滴定管;②如果不进行气密性检查,可能在实验过程中出现漏气,进而导致环境污染等;
(1)①用pH试纸测定Na2CO3溶液的pH,可用玻璃棒蘸取溶液,滴在玻璃片上的pH试纸上观察,故不选;②进行浓硫酸的脱水性实验,应用玻璃棒不断搅拌,故不选;③将适量氯化铁饱和溶液滴入沸水中制氢氧化铁胶体不需要使用玻璃棒,故选;④用已知浓度的盐酸和未知浓度的氢氧化钠溶液进行中和滴定实验,通过滴定管进行滴定,无需玻璃棒,故选;⑤做焰色反应实验,用铂丝蘸取待测液,无需使用玻璃棒,故选;答案选③④⑤;
(2)①a.容量瓶有活塞,使用前需要检查是否漏水,故正确;b.冷凝管使用前不需检查是否漏水,故错误;c.碱式滴定管有橡胶和玻璃珠形成的活塞,使用前需检查是否漏水,故正确;d.长颈漏斗使用前不需检查是否漏水,故错误;e.分液漏斗有活塞,使用前需要检查是否漏水,故正确;答案选ace;②如果不进行气密性检查,可能在实验过程中出现漏气,会导致abcd项中的后果,可燃性气体泄漏还可能发生爆炸,故答案为:abcd;(3)a、A中装浓硫酸,B中装浓盐酸,这样的操作是方便A中的液体流下,但是因为流下的浓硫酸的量少,不可能一下子全部吸收完浓盐酸中的水分,得不到干燥的纯净气体,错误;b、A中装浓盐酸,B中装浓硫酸,这样当有少量的浓盐酸流下来时,就会被大量的浓硫酸吸收完里面的水份,从而得到干燥的纯净的氯化氢气体,正确;c、A中装氢氧化钠浓溶液,B中装浓氨水,得不到干燥的纯净气体,错误;d、A中装浓氨水,B中装氢氧化钠浓溶液,得不到干燥的纯净气体,错误。答案选b。


 教学练新同步练习系列答案
教学练新同步练习系列答案 课前课后同步练习系列答案
课前课后同步练习系列答案科目:高中化学 来源: 题型:
【题目】分析、归纳、探究是学习化学的重要方法和手段之一。下面就电解质A回答有关问题 (假定以下都是室温时的溶液)。
(1)电解质A的化学式为NanB,测得浓度为c mol/L的A溶液的pH=a
①当a =10时,A溶液呈碱性的原因是(用离子方式程式表示)___________________。
②当a =11,n =1时,A溶液中各种离子浓度由大到小的顺序为_____________________, c(OH-)-c(HB)=________ mol/L。
③当n=1、c=0.1,溶液中c(HB)∶c(B-)=1∶999时,A溶液的pH为______(保留整数值)。
(2)已知难溶电解质A的化学式为XY2,测得其饱和溶液中X2+离子的浓度为c mol/L,则该难溶物XY2的溶度积常数为Ksp=_______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是模拟“侯氏制碱法”制取NaHCO3的部分装置。下列操作正确的是

A. a先通入CO2,然后b通入NH3,c中放碱石灰
B. a先通入NH3,然后b通入CO2,c中放蘸稀硫酸的脱脂棉
C. b先通入NH3,然后a通入CO2,c中放碱石灰
D. b先通入CO2,然后a通入NH3,c中放蘸稀硫酸的脱脂棉
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于各装置图的叙述,不正确的是
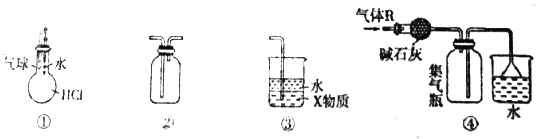
A. 装置①可验证HCl气体在水中的溶解性
B. 装置②可用于收集H2、Cl2、NO2、NO等气体
C. 装置③中X为四氯化碳时,可用于吸收氨气或氯化氢
D. 装置④可用于干燥、收集并吸收多余的氨气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组研究溶液中AgNO3和Na2S的反应。
实验 | 试剂 | 现象 | |
| 试管 | 滴管 | |
(pH = 4) |
(pH = 9) | 出现黑色沉淀 | |
(1)用离子方程式解释Na2S溶液pH > 7的原因:________。
(2)实验小组同学认为黑色沉淀中可能含有Ag2O、Ag2S或Ag,设计实验验证。
已知:i.浓硝酸能将Ag2S转化为![]() 和
和![]() ;
;
ii.Ag2O能溶解在浓氨水中形成银氨溶液,而Ag2S和Ag均不能。
① 设计并实施如下实验,证实沉淀中含有Ag2S。

试剂1和试剂2分别是_________、_________。
现象1和现象2分别是_________、_________。
② 设计并实施如下实验,证实沉淀中不含有Ag2O,将实验操作和现象补充完整。
实验操作 | 实验现象 | |
步骤i | 取少量银氨溶液,向其中滴加盐酸 | 出现白色沉淀 |
步骤ii | 取少量洗涤后的黑色沉淀,____________ | ____________ |
③ 经检验,沉淀不含有Ag。

(3)实验小组同学认为AgNO3溶液具有氧化性,在一定条件下能够氧化Na2S,设计实验进行研究(实验装置如右图所示),测得电压为a(![]() )。
)。
对AgNO3溶液中氧化![]() 的物质进行推测:
的物质进行推测:
假设1: ![]() 的AgNO3溶液中
的AgNO3溶液中![]() 氧化了
氧化了![]() ;
;
假设2: ![]() 的AgNO3溶液中
的AgNO3溶液中![]() 氧化了
氧化了![]() 。
。
利用右图装置继续研究(已知:电压大小反映了物质氧化还原性强弱的差异;物质氧化性与还原性强弱差异越大,电压越大)。
① 将![]() 的AgNO3溶液替换为_______溶液,记录电压为b(
的AgNO3溶液替换为_______溶液,记录电压为b(![]() )。
)。
② 上述实验证实了氧化![]() 的物质中一定包含
的物质中一定包含![]() ,其证据是______。
,其证据是______。
实验结论:AgNO3溶液与Na2S溶液的反应类型与反应条件有关。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】自热食品已成为现代生活的时尚。自热食品包装中有两包发热剂,在这两包发热剂中最适合盛放的物质是( )
A. 浓硫酸和水 B. 氯化铵和氢氧化钡晶体 C. 氯化钠和水 D. 生石灰和水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在离子 RO3n 中, 共有 x 个核外电子,R 原子的质量数为 A,则 R 原子核内含有的中子数目是( )
A. A-x+n+24 B. A-x+n+48
C. A-x-n-24 D. A+x-n-24
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物的表示方法多种多样,下面是常用的有机物的表示方法:
①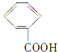 ②
②![]() ③CH4 ④
③CH4 ④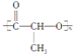 ⑤
⑤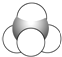
⑥ ⑦
⑦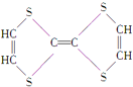
⑧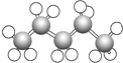 ⑨
⑨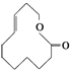 ⑩
⑩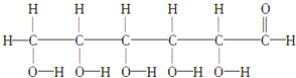
(1)上述表示方法中属于结构简式的为 _________;属于结构式的为 _______________;属于键线式的为 ________________;属于比例模型的为 _______________;属于球棍模型的为 __________________;
(2)写出⑨的分子式: ________________;
(3)②的分子式为 ________________,最简式为 ______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在无色透明的强酸性溶液中能大量共存的是( )
A.K+、Na+、OH-、Cl﹣
B.Na+、K+、Cl﹣、SO42-
C.Ca2+、Na+、CO32-、NO3-
D.Cu2+、SO42-、Mg2+、NO3-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com