
【题目】【2016届唐山二模】目前人们对环境保护、新能源开发很重视。
(1)汽车尾气中含有CO、NO2等有毒气体,对汽车加装尾气净化装置,可使有毒气体转化为无毒气体。
4CO(g)+2NO2(g) ![]() 4CO2(g)+N2(g) ΔH=-1200 kJ·mol-1
4CO2(g)+N2(g) ΔH=-1200 kJ·mol-1
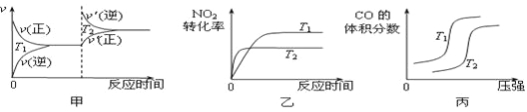
对于该反应,温度不同(T2>T1)、其他条件相同时,下列图像正确的是 (填代号)。
(2)用活性炭还原法也可以处理氮氧化物,某研究小组向某密闭容器加入一定量的活性炭和NO,发生反应C(s)+2NO(g) ![]() N2(g)+CO2(g) ΔH在T1℃时,反应进行到不同时间测得各物质的量浓度如下:
N2(g)+CO2(g) ΔH在T1℃时,反应进行到不同时间测得各物质的量浓度如下:
浓度/(mol/L) | 0 | 10 | 20 | 30 | 40 | 50 |
NO | 1.0 | 0.58 | 0.40 | 0.40 | 0.48 | 0.48 |
N2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
CO2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
①根据图表数据分析T1℃时,该反应在0-20min的平均反应速率v(CO2)= ;计算该反应的平衡常数K= 。
②30min后,只改变某一条件,根据上表的数据判断改变的条件可能是 (填字母代号)。
A.加入一定量的活性炭 B.通入一定量的NO
C.适当缩小容器的体积 D.加入合适的催化剂
③若30min后升高温度至T2℃,达到平衡时,容器中NO、N2、CO2的浓度之比为5:3:3,则达到新平衡时NO的转化率 (填“升高”或“降低”),ΔH 0(填“>”或“<”).
(3)以CO2与NH3为原料可合成化肥尿素[化学式为CO(NH2)2]。已知:
①2NH3(g)+CO2(g)=NH2CO2NH4(s) ΔH= -l59.5kJ/mol
②NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g) ΔH= +116.5kJ/mol
③H2O(l)=H2O(g) ΔH=+44.0kJ/mol
写出CO2与NH3合成尿素和液态水的热化学反应方程式 。
(4)一种氨燃料电池,使用的电解质溶液是2mol/L的KOH溶液。
电池反应为:4NH3+3O2=2N2+6H2O;
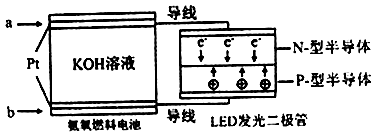
请写出通入a气体一极的电极反应式为 ;每消耗3.4g NH3转移电子的物质的量为 。
【答案】(14分)(除标明外每空2分) (1)乙(1分);
(2)①0.015 mol·L-1 ·min-1 (1分); 0.56 (或9/16)②bc ;③降低(1分); < (1分);
(3)2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(l) ΔH= –87.0 kJ·mol-1
(4)2NH3+6OH-– 6e-=N2 + 6H2O 0.6 mol
【解析】
试题分析:(1)甲:升高温度,化学平衡逆向移动,化学反应速率会迅速增大,会离开原来的速率点,错误;乙:升高温度,化学反应速率会迅速增大,所以T2 时先达到化学平衡状态,并且由于该反应的正反应是放热反应,所以升高温度,化学平衡向吸热的逆反应方向移动,使二氧化氮的转化率减小,正确;丙:对于该反应来说,正反应是气体体积减小的反应,在温度不变时,增大压强,平衡正向移动,一氧化碳的体积分数会减小,错误;(2) ①根据表格数据可知:在20min内CO2的浓度增大0.30mol/L,则用CO2的浓度改变表示反应速率是V(CO2)=0.30mol/L÷20min=0.015mol/(L·min);反应达到平衡时,各种物质的浓度分别是:c(NO)=0.48mol/L;c(N2)=c(CO2)=0.36mol/L,所以在该温度下的化学平衡常数K= c(N2)·c(CO2)÷c2(NO)= (0.36mol/L ×0.36mol/L )÷(0.48mol/L)2=9/16=0.56;②30min后,只改变某一条件,反应重新达到平衡,依据图表数据分析,平衡状态各物质浓度增大,而平衡常数只随温度变化,平衡常数不变说明改变的条件一定不是温度;依据数据分析,氮气浓度增大,二氧化碳和一氧化氮浓度增大,反应前后气体体积不变,所以可能是减小溶液体积或加入一定量一氧化氮;故答案为bc;③在原来平衡时,c(NO):c(N2):c(CO2)= 0.48:0.36:0.36=4:3:3,若30min后升高温度至T2℃,达到平衡时,容器中NO、N2、CO2的浓度之比为5:3:3,氮气和二氧化碳浓度之比始终为1:1,所以5:3>4:3,说明平衡向逆反应方向移动,升高温度平衡逆向移动,根据平衡移动原理:升高温度,化学平衡向吸热的反应方向移动,说明逆反应是吸热反应,则正反应是放热反应,故△H<0;(3)依据热化学方程式和盖斯定律计算①+②-③得到CO2与NH3合成尿素和液态水的热化学反应方程式为2NH3(g)+CO2(g)=CO(NH2)2(s)+H2O(l) ΔH= –87.0 kJ·mol-1;(4) 电池反应为:4NH3+3O2=2N2+6H2O.该电池负极是氨气失电子生成氮气,根据示意图可知a电极是负极,发生氧化反应,发生的电极反应式为2NH3+6OH-– 6e-=N2 + 6H2O,反应中2mol氨气反应电子转移6mol电子,每消耗3.4g NH3的物质的量=13.4g÷17g/mol=0.2mol,所以转移的电子数为0.36NA 。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】下列变化属于加成反应的是
A.乙烯通入酸性高锰酸钾溶液中
B.乙烯通入溴水中
C.苯与液溴在FeBr3催化下反应
D.甲烷与氯气在一定条件下反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【2016届雅安三诊】利用I2O5可消除CO污染,反应为I2O5(s)+5CO(g)![]() 5CO2(g)+I2(s)。不同温度下,向装有足量的I2O5固体的2L恒容密闭容器中通入2mol CO,测得CO2 的体积分数ψ(CO2)随时间t变化曲线如下图,下列说法正确的是
5CO2(g)+I2(s)。不同温度下,向装有足量的I2O5固体的2L恒容密闭容器中通入2mol CO,测得CO2 的体积分数ψ(CO2)随时间t变化曲线如下图,下列说法正确的是
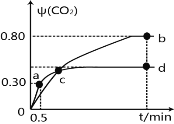
A.b点时,CO的转化率为20%
B.容器内的压强保持恒定,表明反应达到平衡状态
C.b点和d点的化学平衡常数:Kb>Kd
D.0到0.5min反应速率v(CO)=0.3mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在浓度为0.01mol/L Mg(HCO3)2,0.02mol/LCaCl2的水溶液1L中,要同时除去Mg2+,Ca2+应选用的试剂是( )
A. NaHCO3 B. Na2CO3 C. Ca(OH)2 D. NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】美国普度大学研究开发出一种利用铝镓合金制备氢气的新工艺(如图所示)。下列有关该工艺的说法错误的是( )

A.该过程中,能量的转化形式只有两种
B.铝镓合金可以循环使用
C.铝镓合金与水反应的化学方程式为2Al+3H2O=Al2O3+3H2↑
D.总反应式为2H2O![]() 2H2↑+O2↑
2H2↑+O2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】原电池发生的反应是可自发进行的氧化还原反应,CO/O2燃料电池以熔融状态的碳酸盐为电解质,下列说法正确的是 ( )
A、CO在正极通入
B、CO32— 在电池内部向正极移动
C、当有22.4LCO参加反应时电路中有2mol电子发生转移
D、该电池电解质在固态时,电池无法工作
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水杨酸是合成阿司匹林的重要原料。水杨酸的学名邻羟基苯甲酸,结构简式为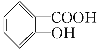 ,请回答下列问题:
,请回答下列问题:
(1)请写出水杨酸中具有的官能团名称________;
(2)能够区分水杨酸和苯酚的试剂_____ ___;
A.浓溴水 B.氢氧化钠溶液 C.氯化铁溶液 D.碳酸氢钠溶液
(3)水杨酸的另一种同分异构体的结构简式为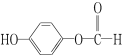 ,1 mol该有机物在适宜条件下与氢氧化钠经过一系列反应,最多能消耗氢氧化钠的物质的量为(填序号)________;
,1 mol该有机物在适宜条件下与氢氧化钠经过一系列反应,最多能消耗氢氧化钠的物质的量为(填序号)________;
A.1 mol B.2 mol C.3 mol D.4 mol
(4)已知有机物CH3COOH可以表示为:![]() ,在一定条件下,水杨酸与乙酸酐可合成阿司匹林,阿司匹林可表示为:
,在一定条件下,水杨酸与乙酸酐可合成阿司匹林,阿司匹林可表示为: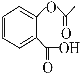 ,则阿司匹林分子式为________;
,则阿司匹林分子式为________;
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验是实现科学探究的重要途径。
(1)下列关于教材实验的叙述中正确的是
A.Cu片加入冷的浓硫酸中没有变化,说明Cu在浓硫酸中也会钝化
B.石油分馏时,控制温度,收集到的汽油为纯净物
C.用激光笔照射肥皂水,有丁达尔效应,说明肥皂水是胶体
D.淀粉水解液中加入银氨溶液,水浴加热后无银镜,说明淀粉未水解
E.鸡蛋白溶液中分别加入饱和硫酸铵、硫酸钾溶液时,都发生了盐析
(2)某兴趣小组设计出下图装置(气密性已检查),验证铜与稀硝酸反应的产物。
已知:FeSO4+NO=[Fe(NO)]SO4,该反应较缓慢,待生成一定量[Fe(NO)]2+时突显明显棕色。
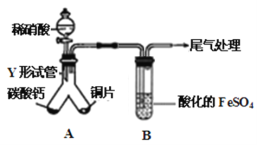
①实验开始时先将Y形试管向盛有碳酸钙的支管倾斜,缓慢滴入稀硝酸,该实验操作的目的是 。
②由分液漏斗向Y形试管右侧加入稀硝酸,反应的离子方程式是
。
③本实验A生成的气体中,若有NO2,B的实验现象为 ;若只有NO生成,B的实验现象是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向有机物X中加入合适的试剂(可以加热),检验其官能团。下列有关结论不正确的是:( )
选项 | 试剂 | 现象 | 结论 |
A | 金属钠 | 有气体产生 | 含羟基 或羧基 或羟基和羧基 |
B | 银氨溶液 | 产生银镜 | 含有醛基 |
C | 碳酸氢钠溶液 | 产生气泡 | 含有羧基 |
D | 溴水 | 溶液褪色 | 含有碳碳双键 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com