
【题目】《本草经集注》中记载有关于区别硝石(KNO3)和朴硝(Na2SO4) 的方法:“强烧之,紫青烟起,…,云是真硝石也。”文中区别的方法是利用了下列中的( )
A. 焰色反应 B. 萃取 C. 丁达尔效应 D. 蒸馏
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】将一定量的CO2气体通入2L的NaOH溶液中,在所得溶液中逐滴加入稀盐酸至过量,并将溶液加热,产生的气体与消耗的HC1物质的量关系如图所示(忽略气体的溶解和HC1的挥发).下列说法不正确的是
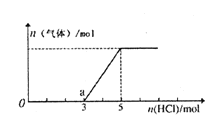
A. 0点溶液中所含溶质的化学式为NaOH、Na2CO3
B. 0到a点发生反应的离子方程式:H++OH-=H2O、CO32-+H+=HCO3-
C. 通入CO2气体的体积在标准状况下为22.4L
D. NaOH溶液的物质的量浓度为2.5mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 元素周期表有18个纵行,每一个纵行是一族
B. 34号元素位于第四周期VA族
C. 只有一种元素组成的物质一定是纯净物
D. 同素异形体之间的相互转化属于化学反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化铝(AIN)是一种新型无机非金属材料。某AlN样品仅含有趾Al2O3杂质,为测定AlN的含量,设计如下三种实验方案。
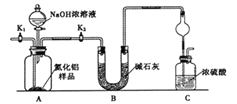
(1)上图C装置中球形干燥管的作用是_____________________。
(2)实验步骤:组装好实验装置,检查好装置气密性再加入实验药品,接下来关闭K1,打开K2,打开分液漏斗活塞,加入NaOH浓溶液,至不再产生气体。打开K1,通入氮气一段时间,测定C装置反应前后的质量变化,通入氮气的目的____________________。
(3)由于装置存在缺陷,导致测定结果偏高,请提出改进意见__________________。
【方案2】用如图装置测定mg样品中A1N的纯度(部分夹持装置已略去)。
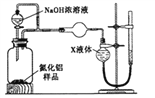
(4)为测定生成气体的体积,量气装置中的X液体不可以是_____________________。
A.NH4Cl溶液 b.CCl4 c.H2O d.苯
(5)若ag样品完全反应,测得生成气体的体积为bmL(已转换为标准状况),则AlN的质量分数是__________。
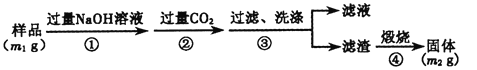
(6)写出步骤中发生的化学反应方程式_______________________________。
(7)若在步骤③中未洗涤,测定结果将______(填“偏高”、“偏低”或“无影响”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】区别浓硫酸与稀硫酸,既简单又可靠的方法是( )
A. 各取少许溶液分别放入铜片 B. 分别与石蕊溶液作用
C. 各取少许溶液加入BaCl2溶液 D. 各取少许溶液分别放入铁片
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将 1mol X 和 2mol Y 充入容积为 1L 的密闭容器中,分别在 250℃和 T℃下发生反应:X(g)+2Y(g)![]() Z(g) △ H,Z 的物质的量随时间变化如右图。下列说法正确的是( )
Z(g) △ H,Z 的物质的量随时间变化如右图。下列说法正确的是( )
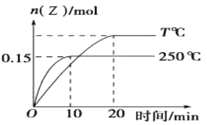
A. △ H > 0
B. 250 ℃时,0~l0min, v(Y)=0.015mol/(L·min)
C. 其他条件不变若减小容器体积,X 的体积分数增大
D. T℃,20min 时再充入 1molX 和 2molY,重新达到平衡时 Y 的转化率增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于氧化还原反应的叙述中,正确的是( )
A.有单质参加的反应一定是氧化还原反应
B.燃烧反应必须有氧气作氧化剂
C.2Fe+3Cl2═2FeCl3; Fe+S ![]() FeS 由此可以判断氧化性:Cl2>S
FeS 由此可以判断氧化性:Cl2>S
D.Mg在化学反应中失去2个电子,而Al在化学反应中失去3个电子,因此还原性Al>Mg
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列为元素周期表的一部分,表中阿拉伯数字(1、2……)是元素周期表中行或列的序号。请参照元素A~I在表中的位置,回答下列问题。
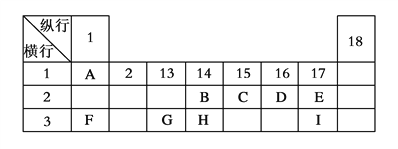
(1)B、C、H三元素中非金属性最强的是________(写出元素名称),写出AF化合物的电子式__________,若AF与水反应产生2.24L气体(标准状况下),则转移电子数目为_______。
(2)表中某元素能形成两性氧化物,写出该氧化物溶于氢氧化钠溶液的离子方程式: ____________。
(3)表中某元素的单质在常温下为气态,该元素能与A~I中的一种元素构成原子个数比为1:1和1:2的两种共价化合物X和Y,该元素还能与A~I中的另一种元素构成原子个数比为1:1和1:2的两种离子化合物Z和M。写出Z与Y反应的化学方程式:_____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】洪灾过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一.漂白粉是常用的消毒剂.
(1)工业上将氯气通入石灰乳[Ca(OH)2]制取漂白粉,漂白粉的有效成分是(填化学式)有关化学反应方程式为 .
(2)漂白粉溶于水后,受空气中的CO2作用,即产生有漂白、杀菌作用的次氯酸,化学反应方程式为 .
(3)O3与Cl2具有相似的性质,均可用于自来水的消毒.已知二者在消毒时均被还原为最低价态,则相同状况下10L O3与L Cl2的消毒能力相当.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com