
科目:高中化学 来源:2015-2016学年山西省运城市高二上学期单元测4化学试卷(解析版) 题型:选择题
膦(PH3)又称磷化氢,在常温下是一种无色有大蒜臭味的有毒气体,电石气的杂质中常含有磷化氢.它的分子构型是三角锥形.以下关于PH3的叙述正确的是( )
A.PH3分子中有未成键的孤对电子
B.PH3是非极性分子
C.PH3是一种强氧化剂
D.PH3分子的P﹣H键是非极性键
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东省临沂市高一下第二次月考化学试卷(解析版) 题型:选择题
在如图所示的原电池中,下列说法正确的是( )
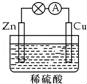
A.负极发生还原反应
B.正极反应为 Cu﹣2e﹣═Cu2+
C.电子由铜片通过导线流向锌片
D.反应一段时间后,溶液的酸性减弱
查看答案和解析>>
科目:高中化学 来源:2015-2016学年福建省漳州市高二下期中理科化学试卷(解析版) 题型:选择题
下列物质与NaOH醇溶液共热完全反应后,可得3种有机物的是( )
A.CH3﹣CHCl﹣CH2﹣CH3
B.
C.CH3﹣C(CH3)Cl﹣CH2﹣CH3
D.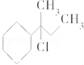
查看答案和解析>>
科目:高中化学 来源:2015-2016学年福建省漳州市高二下期中理科化学试卷(解析版) 题型:选择题
下列反应中不能引入羟基(﹣OH)的是( )
A.加成反应 B.取代反应 C.消去反应 D.还原反应
查看答案和解析>>
科目:高中化学 来源:2015-2016学年安徽省阜阳市高一下第二次月考化学试卷(解析版) 题型:实验题
某化学兴趣小组为探究元素性质的递变规律,设计了如下系列实验。
Ⅰ.(1)将钠、钾、镁、铝各1 mol分别投入到足量的0.1 mol·L-1的盐酸中,试预测实验结果:________________与盐酸反应最剧烈,
(2)将NaOH溶液与NH4Cl溶液混合生成NH3·H2O,从而验证NaOH的碱性大于NH3·H2O,继而可以验证Na的金属性大于N,你认为此设计是否合理______________?并说明理由:_____________________。
Ⅱ.利用下图装置可以验证非金属性的变化规律。
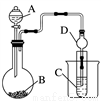
(3)仪器A的名称为____________,干燥管D的作用是______________。
(4)实验室中现有药品Na2S、KMnO4、浓盐酸、MnO2,请选择合适药品设计实验验证氯的非金属性大于硫:装置B、C中所装药品分别为____________、________,装置C中的实验现象为有淡黄色沉淀生成,离子方程式为________________。
(5)若要证明非金属性:C>Si,则A中加________、B中加Na2CO3、C中加________,观察到C中溶液的现象为_________________________________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年安徽省阜阳市高一下第二次月考化学试卷(解析版) 题型:选择题
已知断开1mol H﹣H键要吸收436kJ的能量,断开1mol Cl﹣Cl键要吸收243kJ的能量,而形成1mol H﹣Cl键要放出431kJ的能量,对于反应:H2+Cl2═2HCl,下列说法正确的是( )
A.该反应在发生过程中要吸收能量
B.该反应在发生过程中要放出能量
C.反应后若生成2 mol HCl,则一定会放出2×431 kJ的能量
D.断开1 mol H﹣H键要吸收的能量与形成1 mol H﹣Cl键要放出的能量相等
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省唐山市高二(上)质检化学试卷(解析版) 题型:选择题
下列各组有机物中,其一氯代物的数目不相等的是( )
A. 正戊烷和正己烷
B. 苯和乙烷
C. 对二甲苯和2,2﹣二甲基丙烷
D. 甲苯和2﹣甲基丁烷
查看答案和解析>>
科目:高中化学 来源:2016届宁夏高三上模拟五化学试卷(解析版) 题型:填空题
工业制硝酸的主要反应为:4NH3(g)+5O2(g)?4NO(g)+6H2O(l)△H
(1)已知氢气的燃烧热为△H=﹣285.8kJ/mol.
N2(g)+3H2(g)═2NH3(g)△H=﹣92.4kJ/mol;
N2(g)+O2(g)═2NO(g)△H=+180.6kJ/mol.
则上述工业制硝酸的主要反应的△H= .
(2)在容积固定的密闭容器中发生上述反应,容器内部分物质的物质的量浓度如表:
浓度 | c(NH3)(mol/L) | c(O2)(mol/L) | c(NO)(mol/L) |
起始 | 0.8 | 1.6 | 0 |
第2min | 0.6 | a | 0.2 |
第4min | 0.3 | 0.975 | 0.5 |
第6min | 0.3 | 0.975 | 0.5 |
第8min | 0.7 | 1.475 | 0.1 |
①反应在第2min到第4min时,O2的平均反应速率为 .
②反应在第6min时改变了条件,改变的条件可能是 (填序号).
A.使用催化剂 B.升高温度 C.减小压强 D.增加O2的浓度
③下列说法中能说明4NH3(g)+5O2(g)?4NO(g)+6H2O(g)达到平衡状态的是 (填序号).
A.单位时间内生成n mol NO的同时,生成n mol NH3
B.条件一定,混合气体的平均相对分子质量不再变化
C.百分含量w(NH3)=w(NO)
D.反应速率v(NH3):v(O2):v(NO):v(H2O)=4:5:4:6
E.若在恒温恒压下容积可变的容器中反应,混合气体的密度不再变化
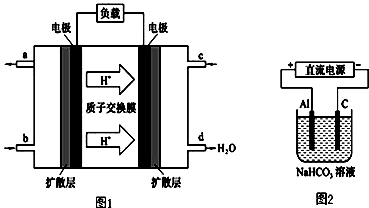
(3)某研究所组装的CH2=CH2﹣O2燃料电池的工作原理如图1所示.
①该电池工作时,b口通入的物质为 .
②该电池负极的电极反应式为: .
③以此电池作电源,在实验室中模拟铝制品表面“钝化”处理(装置如图2所示)的过程中,发现阳极周围变浑浊并有气泡产生,其原因可能是: (用相关的离子方程式表示).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com