
��11�֣�ͭ���������ϵ�dz����еij���������
����֪�����£�����Һ��Cu2+�ȶ���Cu+�������������·�����Ӧ��2Cu+ = Cu2++ Cu��
��1��CuH��HԪ�ػ��ϼ�Ϊ ��
��2��Ŀǰ�Ʊ�����Cu2O��һ�ַ���:��������ͭ����Һ�е���N2H4��H2Oˮ��Һ����ַ�Ӧ�ɵõ�Cu2O��ͬʱ������ɫ��ζ�����塣�����Ʊ��������ܷ�Ӧ�Ļ�ѧ����ʽΪ ��
��3��һ�������£���CuSO4�м���NH4H��Ӧ�����⻯��ͭ��CuH������CuH�ܽ�������ϡ�����У�������6.72 L H2����״���£�ʱ���μӷ�Ӧ����������ʵ���Ϊ ��
��ȸʯ����ɫ����һ������ı�ʯ������Ҫ�ɷ���xCu��OH��2��yCuCO3��ij��ȤС��Ϊ̽����ȸʯ��ɣ�������ͼ��ʾ��װ�ã��г�����ʡ�ԣ�����ʵ�飺

����1�����װ�õ������ԣ�����ϸ����Ʒ����Ӳ�ʲ������С�
����2���������װ�õ�����������K�����������һ��ʱ���رա�
����3������װ��Bֱ��װ��C�������ݲ�����
����4��_________________________��
����5����ȴ�����£��������װ�õ�������
��1���벹�䲽��4�������ݣ�_____________________________��
��2������װ��E����ʵ��ⶨ��x/y��ֵ��__________��ѡ�ƫ����ƫС������Ӱ�족����
��3��ijͬѧ��ʵ������вɼ����������ݣ�
A����ӦǰӲ�ʲ���������Ʒ������163.8g
B����Ӧ��Ӳ�ʲ������в�����������20g
C��װ��Cʵ�������2.25g
D��װ��Dʵ�������5.5g
Ϊ�ⶨx/y��ֵ������Ϊ����ѡ���������ɼ������е�_______________��д��������ϵ���ĸ���ţ���һ�鼴�ɽ��м��㣬��������ļ�������д����ȸʯ��ɵĻ�ѧʽ____________��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�����ʡ��һ�϶��п��Ի�ѧ�Ծ��������棩 ���ͣ������
��ֻ��ͨ����ѧ����𣬴���ⲻ���֣���18�֣�
��1���������������ʢ�ˮ���ƾ���ú��ʯ�� ��CaO��SO3��SO2��P2O5 ��HNO3��H2SO4��HCl��NaCl ��KClO3��KCl��KMnO4��HgO�����о���һ����������������������ʲ�ͬ�����������ʷֱ��ǣ���__________����______ __����_______����__________��
��2������״����22��4 L��HCl ����ˮ���200 mL����Һ��������Һ�����ʵ���Ũ��Ϊ__________mol/L��
��3��3��01��1023��OH-�����ʵ���Ϊ___________mol������Ϊ___________g�����е��ӵ����ʵ���Ϊ___________mol����ЩOH-��___________mol NH3��������ͬ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ���ຣʡ�߶���9���ʼ컯ѧ�Ծ��������棩 ���ͣ�ѡ����
��֪H2��g��+ Cl2��g�� === 2HCl��g�� ��H= -184��6KJ?mol-1,��HCl��g��==1/2H2��g��+1/2Cl2��g���ġ�HΪ
A��+184��6KJ?mol-1 B��92��3KJ?mol-1
C��-369��2KJ?mol-1 D��+92��3KJ?mol-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ������һ�и�һ��ѧ��10���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
����˵����ȷ����
A����״����44.8L�Ҵ�������ԭ����Ϊ12NA
B��1mol��������ֻ���ڱ�״���²���22.4L
C�����³�ѹ�£���������N2��N4��������ԭ������ͬ
D����״����1.12L CO��N2�Ļ�����庬��Լ3.01��1022��ԭ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�������ʡ������ѧ�����в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
��NAΪ�����ӵ�������ֵ������˵����ȷ����
A��һ�������£�0.1mol SO2������������Ӧ����SO3��ת�Ƶ�����Ϊ0.2NA
B����״���£�20g D2O����������������Ϊ10NA
C����״���£�22.4L Cl2��ȫ����ˮ�γ���ˮʱ��ת�Ƶ�����ΪNA
D������ȼ�ϵ����������22.4L����ʱ����·��ͨ���ĵ�����ĿΪ4NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�������˫Ѽɽ��һ��ѧ������ѧ�����в��Ի�ѧ�Ծ��������棩 ���ͣ������
��10�֣���1�� P2O5�Ƿ������Ը�������������岻����Ũ����������P2O5�������______
a��NH3 b��HI c��SO2 d��CO2
��2����ҵ�����״��ij��÷����ǣ�CO��g��+2H2��g�� CH3OH��g�� ��H1 = ��90.8kJ/mol��
CH3OH��g�� ��H1 = ��90.8kJ/mol��
��֪��2H2��g��+O2��g��=2H2O��l�� ��H2 = -571.6kJ/mol��
2CO��g��+O2��g��=2CO2��g�� ��H3= -566.0kJ/mol
����2CH3OH��g��+3O2��g��=2CO2��g��+4H2O��l�� ��H4 = ��
��3���ڼ���п����У��ø��������Ϊ�������ϣ���ط�ӦΪ��2K2FeO4 + 3Zn == Fe2O3 +ZnO +2K2ZnO2
�õ�����������ķ�Ӧ�ĵ缫��ӦʽΪ ��
II������ͼ��ʾװ�ý���ʵ�顣ʵ������У������������������Y������Һ����Ϻ�ɫ��ֹͣʵ�飬���缫���Ա�ϸ�����Һ��Ȼ���塣
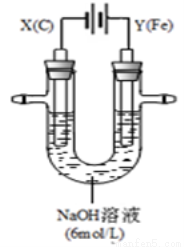
�������Ϸ��֣����������FeO42-������Һ�г��Ϻ�ɫ��
��4���������У�X������Һ��pH ������� ������С�����䡱����
��5���������У�Y�������ĵ缫��ӦΪFe - 6e- + 8OH-��FeO42- + 4H2O �� ��
��6������X���ռ���672 mL���壬��Y���ռ���168 mL���壨��������Ϊ��״��ʱ�������������Y�缫�����缫���������� g��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016��㶫ʡ�����и�����ѧ�ڵڶ����¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
�������ӷ���ʽ��ȷ����
A��Cl2ͨ��ˮ�У�Cl2+H2O = 2H++Cl-+ClO-
B��˫��ˮ����ϡ�����KI��Һ��H2O2��2H����2I��=I2��2H2O
C��Na2O2����ˮ����O2��Na2O2��H2O=2Na����2OH����O2��
D��Na2S2O3��Һ�м���ϡ���2S2O32����4H��=SO42����3S����2H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016��ӱ�ʡ������ѧ�����в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
������ͼ��ʾװ�ý�������ʵ�飬�ܵó���Ӧʵ����۵���
ѡ�� | �� | �� | �� | ʵ����� |
|
A | Ũ���� | MnO2 | NaOH | ������������β�� | |
B | Ũ���� | ���� | ��ˮ | Ũ���������ˮ�ԡ������� | |
C | ϡ���� | Na2SO3 | Ba��NO3��2��Һ | SO2������Ա��ξ������ɰ�ɫ���� | |
D | Ũ���� | Na2CO3 | Na2SiO3��Һ | ���ԣ����̼����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016���Ĵ�ʡ������ѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ʵ����
��15�֣� Ϊ̽����ҵ���ϵ������ã�ij��ѧ��ȤС�����������ʵ�����̣��ú�����������ͭ�ĺϽ������ȡ�Ȼ������̷����壨FeSO4��7H2O���͵������塣

��ش�
��1��д�������Ӧ�����ӷ���ʽ�� ��
��2���Լ�X�� ��������о�����е�ʵ������� ��
��3�����в����ʱ����С������ͼ��ʾװ�ü��Լ���ȡCO2�����Ƶõ�����ͨ����ҺA�С�һ��ʱ��۲쵽�ձ��в����İ�ɫ���������١�Ϊ�˱������C���٣��ɲ�ȡ�ĸĽ���ʩ�� ��
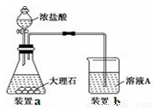
��4���ù���F�Ʊ�CuSO4��Һ���������������;����

д��;�����з�Ӧ�����ӷ���ʽ ��
��ѡ������Ϊ�����;�� ˵��ѡ������� ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com