
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是
A. 27g铝箔在酒精灯上充分加热反应转移电子总数是3NA
B. 2.0gCO2与SO2的混合气体分子中,含有的质子数为NA
C. 25℃时,Ksp(BaSO4)=1×1010,则BaSO4饱和溶液中Ba2+数目为1×105NA
D. 7.8gNa2O2中含有的阴、阳离子的总数为0.4NA
科目:高中化学 来源: 题型:
【题目】对于可逆反应4NH3+5O2![]() 4NO+6H2O(g),下列叙述不正确的是 ( )
4NO+6H2O(g),下列叙述不正确的是 ( )
A.达到平衡时,4v(O2)正=5v(NO)逆
B.达到平衡状态后,NH3 、O2 、NO 、H2O(g)的物质的量保持不变。
C.达到平衡状态时,若增加容器体积,则反应速率增大
D.若单位时间生成xmolNO的同时,生成xmolNH3,则反应达到平衡状态
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化硅(Si3N4)是一种重要的结构陶瓷材料,可用作LED的基质材料,通过等离子法由SiH4(沸点-111.9℃)与氨气反应制取的方程式如下:3SiH4+4NH3=Si3N4+12H2。设NA是阿伏加德罗常数的值,下列说法正确的是( )
A.常温常压下,1.8gSiH4所含质子的数目为3.2NA
B.标准状况下,4.48LNH3和H2的混合气体所含分子总数为0.2NA
C.NA个NH3分子溶于1L的水,所得溶液的物质的量浓度为1mol·L-1
D.当生成1molSi3N4时,转移电子数目为6NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】柠檬酸是无色晶体,无臭、味极酸,分子结构如图所示。广泛用于食品业、化妆业等。其钙盐在冷水中比在热水中易溶解。下列有关柠檬酸的说法不正确的是
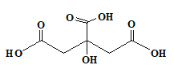
A. 易溶于水,其分子式为C6H8O7
B. 1mol该物质与足量的钠反应最多生成2molH2
C. 利用钙盐溶解性重结晶分离
D. 能作食品抗氧化剂,补酸剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用氨水吸收烟气中的二氧化硫,其相关反应的主要热化学方程式:
SO2(g)+NH3H2O(aq)=NH4HSO3(aq) △H1=a kJmol﹣1
NH3H2O(aq)+NH4HSO3(aq)=(NH4)2SO3(aq)+H2O(l) △H2=b kJmol﹣1
2(NH4)2SO3(aq)+O2(g)=2(NH4)2SO4(aq) △H3=c kJmol﹣1
(1)反应2SO2(g)+4NH3H2O(aq)+O2(g)=2(NH4)2SO4(aq)+2H2O(l)的△H=____kJmol﹣1。
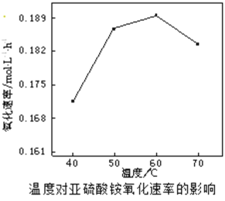
(2)空气氧化(NH4)2SO3的速率随温度的变化如图所示,当温度超过60℃时,(NH4)2SO3氧化速率下降的原因可能是________。
(3)以磷石膏废渣和碳酸铵为原料制备硫酸铵,不仅解决了环境问题,还使硫资源获得二次利用.反应的离子方程式为CaSO4(s)+CO32﹣(aq)SO42﹣(aq)+CaCO3(s),该反应的平衡常数K=________.[已知Ksp(CaCO3)=2.9×10﹣9,Ksp(CaSO4)=9.1×10﹣6]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】目前中国已经通过自主创新成功研发出第一台锌溴液流储能系统,实现了锌溴电池的隔膜、极板、电解液等关键材料自主生产。锌溴电池的原理装置图如图所示,下列说法错误的是( )

A.充电时电极石墨棒A连接电源的正极
B.放电过程中阴离子通过隔膜从正极区移向负极区
C.放电时负极反应为2Br-—2e-=Br2
D.放电时右侧电解质储罐中的离子总浓度增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外兴趣小组成员为研究金属铜与强酸的反应 ,将6.4g铜粉分为两等份,进行了如下实验,请完成有关计算。
(1)取其中一份铜粉投入200mL氢离子浓度为 1molL-1 硫酸和硝酸混合液中,微热使反应充分完成后,生成一氧化氮气体448mL(标准状况)。则反应前混合溶液中硫酸的物质的量浓度为_________(写出计算过程)。
(2)用NaOH溶液吸收氮氧化物是防止NO2污染的一种方法。原理为2NO2 + 2NaOH=NaNO3 + NaNO2 + H2O,NO + NO2 + 2NaOH=2NaNO2 + H2O。取另一份铜粉溶于过量的硝酸溶液,假设硝酸的还原产物只有一氧化氮和二氧化氮,生成的混合气体能被amol NaOH溶液完全吸收,试讨论a的取值范围:_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】白藜芦醇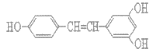 广泛存在于食物(例如桑椹、花生、尤其是葡萄)中,它可能具有抗癌性。下列关于白藜芦醇的说法正确的是
广泛存在于食物(例如桑椹、花生、尤其是葡萄)中,它可能具有抗癌性。下列关于白藜芦醇的说法正确的是
A. 其核磁共振氢谱共有6组峰
B. 能够跟1mol该化合物起反应的Br2或H2的最大用量分别是5mol和7mol
C. 能分别与Na2CO3溶液、FeCl3溶液、NaHCO3溶液、酸性KMnO4溶液反应
D. 所有原子可能共平面
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com