
(12分)下图中,A到L为常见物质或该物质的水溶液,B在A气体中燃烧产生棕色烟,B、G为中学化学中常见金属单质,I的焰色反应为黄色,组成J的元素原子核内只有一个质子,F为无色、有刺激性气味气体,且能使品红溶液褪色。
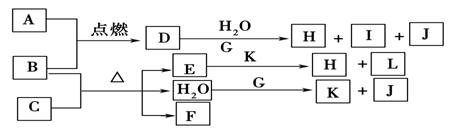
回答下列问题:
(1)K所含的化学键有 。
(2)D的水溶液与G反应的总离子方程式为_______________________________________________。
(3)写出工业上制取单质G的化学方程式 。
(4)将气体F通入下列装置中
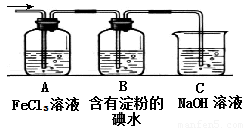
写出A、B中的离子方程式:
、 。
(5)若将F通入一定量K的水溶液中,则所得溶液中各离子浓度一定满足的关系式为
。
(1)离子键、共价键(2)6Na+2Fe3++6H2O===2Fe(OH)3↓+6Na++3H2↑(3)2NaCl 2Na+Cl2↑(4)SO2+2Fe3++2H2O=SO42-+Fe2++4H+
SO2+I2+2H2O=4H++2I-+SO42-(5)c(Na+)+c(H+)=c(OH-)+c(HSO)+2c(SO)
2Na+Cl2↑(4)SO2+2Fe3++2H2O=SO42-+Fe2++4H+
SO2+I2+2H2O=4H++2I-+SO42-(5)c(Na+)+c(H+)=c(OH-)+c(HSO)+2c(SO)
【解析】
试题分析:该题的突破口为B在A中燃烧为棕色的烟,可能为Fe在氯气中燃烧现象;I焰色为黄色,为钠的化合物;J中只有质子为H;F是品红褪色为SO2;结合框图综合考虑可以确定:A为Cl2,B为Fe,C为H2SO4,D为FeCl3,E为Fe2(SO4)3、F为SO2,G为Na,H为Fe(OH)3,I为NaCl,J为H2,K为NaOH,L为Na2SO4;
(1)氢氧化钠含离子键和极性共价键。
(2)钠与氯化铁溶液反应可认为钠先与水反应,生成的氢氧化钠再与氯化铁溶液反应,离子方程式为6Na+2Fe3++6H2O===2Fe(OH)3↓+6Na++3H2↑。
(3)工业上电解熔融氯化钠制钠,方程式为2NaCl 2Na+Cl2↑。
2Na+Cl2↑。
(4)二氧化硫通入氯化铁、碘水中发生氧化还原反应,离子方程式分别为SO2+2Fe3++2H2O=SO42-+Fe2++4H+ SO2+I2+2H2O=4H++2I-+SO42-。
(5)二氧化硫通入氢氧化钠溶液中所得溶质成分可能有四种:亚硫酸钠和氢氧化钠、亚硫酸钠、亚硫酸钠和亚硫酸氢钠、亚硫酸氢钠,无论哪种情况均有电荷守恒:c(Na+)+c(H+)=c(OH-)+c(HSO)+2c(SO)。
考点:无机推断
点评:充分挖掘题眼,利用特征现象、特征反应确定物质。


 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案科目:高中化学 来源: 题型:
(12分)下图类似奥运五元环,表示A、B、C、D、E五种化合物,元环交叉部分代表两种化合物含有一种相同元素,五种化合物由五种短周期元素组成,且每种化合物仅由两种元素组成.A是可燃冰的主要成分;B、E分子中所含电子总数均与硅烷(SiH4)分子的电子数相等,B不稳定,具有较强氧化性,能发生自身氧化还原反应,E的相对分子质量为32,具有还原性,且常用作航天器的燃料; C能发生反应:化合物(Ⅰ)+化合物(Ⅱ) 化合物(Ⅲ)+化合物(Ⅳ);D是新型无机非金属材料,它所含两种元素的原子个数之比为3∶4,电子数之比为3∶2.
(1) D的化学式为________.
(2)A、B、E中含有一种相同的元素,其在周期表中的位置________.
(3)B和E反应可生成单质G和常见的液态化合物H,写出化学方程式__________________.
(4)写出C符合“化合物(Ⅰ)+化合物(Ⅱ) 化合物(Ⅲ)+化合物(Ⅳ)”的化学方程式________________________________.
查看答案和解析>>
科目:高中化学 来源:2013届浙江省杭州市高三上学期期中七校联考化学试卷(带解析) 题型:填空题
(12分)下图中,A到L为常见物质或该物质的水溶液,B在A气体中燃烧产生棕色烟,B、G为中学化学中常见金属单质,I的焰色反应为黄色,组成J的元素原子核内只有一个质子,F为无色、有刺激性气味气体,且能使品红溶液褪色。
回答下列问题:
(1)K所含的化学键有 。
(2)D的水溶液与G反应的总离子方程式为_______________________________________________。
(3)写出工业上制取单质G的化学方程式 。
(4)将气体F通入下列装置中
写出A、B中的离子方程式:
、 。
(5)若将F通入一定量K的水溶液中,则所得溶液中各离子浓度一定满足的关系式为
。
查看答案和解析>>
科目:高中化学 来源: 题型:
(12分)下图中X为中学化学中两种重要单质的混合物。A、G的均为原子晶体,F是正四面体结构的非极性分子,反应②、④是工业上的重要反应。图中部分反应的生成物及反应条件没有列出。

请回答:
(1)写出A和B的化学式:A ,B ;
(2)写出C溶液转化为C固体的过程中![]() 气流的作用是 ;
气流的作用是 ;
(3)写出①、③和④反应的化学方程式:
① ;
③ ;
④ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
(04年江苏卷)(12分)下图中,A是一种无色液体,G是极易溶于水的碱性气体,Y是胃酸的主要成分,K是不溶于稀硝酸的白色沉淀,反应⑤是工业制X的主要反应之一。

请按要求填空:
(1)写出下列物质的化学式:A: ,E: F: ,Y: 。
(2)反应⑤的化学方程式为: 。
(3)1molB通过反应②得到1molF,B中F的质量分数为72%,则B的化学式为:
。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com