
【题目】用18.4 mol·L-1的浓硫酸配制100 mL 1 mol·L-1硫酸。
(1)①应取浓硫酸的体积为__________mL,稀释浓硫酸的操作是_______________________
②若实验仪器有:A.100mL量筒;B.托盘天平;C.玻璃棒;D.50mL容量瓶;E.10mL量筒;F.胶头滴管;G.50mL烧杯;H.100mL容量瓶
实验时必须选用的仪器有(填入编号)___________。
③定容时,若不小心加水超过了容量瓶刻度线,应___________。
(2)该浓硫酸的密度为1.84g·mL-1,据此求出其溶质的质量分数___________。
(3)浓硫酸是中学常用的干燥剂。若100g该浓硫酸能吸收16g水,吸水后生成H2SO4·nH2O,则n=___________。
【答案】5.4mL 用量筒量取浓硫酸后,沿烧杯壁缓缓倒入盛有一定量水的烧杯中,边倒边搅拌 CEFGH 重新配制 98% 1
【解析】
用18.4 mol·L-1的浓硫酸配制100 mL 1 mol·L-1硫酸。
(1)①应取浓硫酸的体积为![]() ,稀释浓硫酸的操作是用量筒量取浓硫酸后,沿烧杯壁缓缓倒入盛有一定量水的烧杯中,边倒边搅拌。
,稀释浓硫酸的操作是用量筒量取浓硫酸后,沿烧杯壁缓缓倒入盛有一定量水的烧杯中,边倒边搅拌。
②若实验仪器有:A.100mL量筒;B.托盘天平;C.玻璃棒;D.50mL容量瓶;E.10mL量筒;F.胶头滴管;G.50mL烧杯;H.100mL容量瓶
实验时必须选用的仪器有10mL量筒、玻璃棒、胶头滴管、.50mL烧杯、100mL容量瓶。
③定容时,若不小心加水超过了容量瓶刻度线,应重新配制。
(2)该浓硫酸的密度为1.84g·mL-1,利用公式![]() 求出溶质的质量分数。
求出溶质的质量分数。
(3)由(2)中求出的浓硫酸的质量分数,求出100g该浓硫酸中含硫酸的质量和水的质量,考虑吸收16g水,然后换算成物质的量,便可求出n值。
(1)①应取浓硫酸的体积为![]() =5.4mL,稀释浓硫酸的操作是用量筒量取浓硫酸后,沿烧杯壁缓缓倒入盛有一定量水的烧杯中,边倒边搅拌。答案为:5.4mL;用量筒量取浓硫酸后,沿烧杯壁缓缓倒入盛有一定量水的烧杯中,边倒边搅拌;
=5.4mL,稀释浓硫酸的操作是用量筒量取浓硫酸后,沿烧杯壁缓缓倒入盛有一定量水的烧杯中,边倒边搅拌。答案为:5.4mL;用量筒量取浓硫酸后,沿烧杯壁缓缓倒入盛有一定量水的烧杯中,边倒边搅拌;
②实验时必须选用的仪器有10mL量筒、玻璃棒、胶头滴管、50mL烧杯、100mL容量瓶。答案为:CEFGH;
③定容时,若不小心加水超过了容量瓶刻度线,应重新配制。答案为:重新配制;
(2)该浓硫酸的密度为1.84g·mL-1,利用公式![]() ,求出溶质的质量分数w%=
,求出溶质的质量分数w%=![]() =
=![]() =98%。答案为:98%;
=98%。答案为:98%;
(3)100g该浓硫酸中含硫酸的质量为100g×98%=98g,含水的质量为100g-98g=2g,考虑吸收16g水,然后换算成物质的量,则n(H2SO4)=1mol,n(H2O)=1mol,很容易求出n=1。
答案为:1。


科目:高中化学 来源: 题型:
【题目】已知下列反应:2CO(g)+O2(g)=2CO2(g) ΔH=-566kJ·mol-1,Na2O2(s)+CO2(g)=Na2CO3(s)+ ![]() O2(g) ΔH=-266kJ·mol-1,试回答:
O2(g) ΔH=-266kJ·mol-1,试回答:
(1)CO的燃烧热ΔH=_______________。
(2)在催化剂作用下,一氧化碳可与过氧化钠反应生成固体碳酸钠,该反应的热化学方程式为:________。
(3)工业废气中的CO2可用碱液吸收,所发生的反应如下:CO2(g)+2NaOH(aq)=Na2CO3(aq)+H2O(l) ΔH=-a kJ·mol-1,CO2(g)+NaOH(aq)=NaHCO3(aq) ΔH=-bkJ·mol-1,则:
①CO2(g)+H2O(l)+Na2CO3(aq)=2NaHCO3(aq)的ΔH=________kJ·mol-1(用含a、b的代数式表示)。
②标况下,11.2LCO2与足量的NaOH溶液充分反应后,放出的热量为_______kJ(用含a或b的代数式表示)。
(4)根据以下三个热化学方程式:2H2S(g)+3O2(g)= 2SO2 (g) +2H2O (l) ΔH=-Q1kJ·mol-1,2H2S(g)+O2(g)= 2S (s) +2H2O (l) ΔH=-Q2kJ·mol-1,2H2S(g)+O2(g)=2 S (s) +2H2O (g) ΔH=-Q3kJ·mol-1,判断Q1、Q2、Q3的大小关系是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组欲探究浓硝酸的性质。
Ⅰ.木炭与浓硝酸反应:
(1)甲同学设计了图1装置,认为若有红棕色气体产生就说明木炭与浓硝酸发生了反应。写出木炭与浓硝酸反应的化学方程式____________________________。

(2)乙同学认为红棕色气体不能作为木炭与浓硝酸反应的证据,其理由是________。
(3)乙同学设计了图2装置实验,木炭能燃烧,并产生红棕色气体。针对该实验现象,乙同学做出如下假设:
假设a:_____________________________;
假设b:红热木炭使HNO3分解产生NO2,NO2可能具有助燃性,木炭燃烧;
假设c:红热木炭使HNO3分解产生O2,木炭与O2反应燃烧;
假设d:红热木炭使HNO3分解产生NO2和O2,共同影响木炭的燃烧;……
(4)设计实验证明假设b成立,请将实验方案补充完整。
①实验方法:_____________________________________________________。
实验现象:木炭在该气体中持续燃烧,火焰迅速变亮,集气瓶中气体颜色变浅直至无色,产生的气体能使澄清石灰水变浑浊,且遇空气不变色。
②根据实验现象写出木炭与此气体反应的化学方程式__________________。
Ⅱ.设计硝酸在不同条件下分解实验,方案见下表:
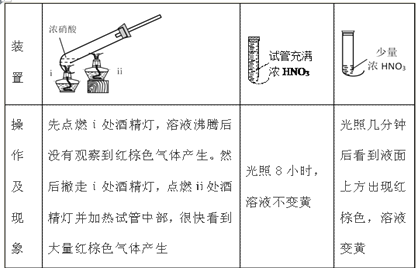
(5)分析上述现象,得出使硝酸成功分解的关键是____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素①~⑩在周期表中的位置如下表所示:
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
1 | ① | ② | ||||||
2 | ③ | ④ | ⑤ | ⑥ | ||||
3 | ⑦ | ⑧ | ⑨ | ⑩ |
回答下列问题:
(1)最外层电子数为2的元素有________(填元素符号);⑨的简单离子结构示意图为________,①与⑥以原子个数比为1:1形成的化合物的电子式为________,用电子式表示⑦与⑩形成化合物的过程________________________。
(
(3)高温灼烧⑦与⑩两种元素形成的化合物时,火焰呈________色。⑧可用于航空航天合金材料的制备,工业上冶炼该单质的化学方程式为________。
(4)④、⑤、⑥的气态氢化物中最稳定的是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各物质所含原子数目,按由大到小顺序排列的是( )
①0.5 mol NH3②标准状况下22.4 L He ③4 ℃ 9 mL水 ④19.6 g H3PO4
A. ①④③② B. ④③②①
C. ②③④① D. ①④②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中含H+、SO42-、NO3-三种离子,其中H+、SO42-的物质的量浓度分别为7.0 mol·L-1和2.0 mol·L-1。取该溶液20 mL,加入3.2 g铜粉,加热使它们充分反应,产生的气体在标准状况下的体积约为( )
A. 0.75 LB. 0.336 LC. 1.5 LD. 0.448 L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有硫酸镁溶液500mL,它的密度是1.20g·cm3,其中镁离子的质量分数是4.8%,则有关该溶液的说法不正确的是
A. 溶质的质量分数是24% B. 溶液的物质的量浓度是2.4mol·L1
C. 溶质和溶剂的物质的量之比约为1∶21.1 D. 硫酸根离子的质量是230.4g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:2Fe2++Cl2===2Cl﹣+2Fe3+,2Br﹣+Cl2===Br2+2Cl﹣,2Fe2++Br2===2Br﹣+2Fe3+。含有amol FeBr2的溶液中,通入xmol Cl2,下列各项为通Cl2过程中,溶液内发生反应的离子方程式,其中不正确的是( )
A. x=0.4a,2Fe2++Cl2===2Fe3++2Cl﹣
B. x=0.6a,2Br﹣+Cl2===Br2+2Cl﹣
C. x=a,2Fe2++2Br﹣+2Cl2===Br2+2Fe3++4Cl﹣
D. x=1.5a,2Fe2++4Br﹣+3Cl2===2Br2+2Fe3++6Cl﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】《本草图经》中关于绿矾的分解有如下描述:“绿矾形似朴消(Na2SO4·10H2O)而绿色,取此物置于铁板上,聚炭,封之囊袋,吹令火炽,其矾即沸,流出,色赤如融金汁者是真也。”对此段话的说明中肯定错误的是( )
A. 绿矾的化学式为FeSO4·7H2O B. 绿矾分解过程中没有发生电子的转移
C. “色赤”物质可能是Fe2O3 D. 流出的液体中可能含有硫酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com