
| A. | 泡利原理 | B. | 能量最低原理 | C. | 洪特规则 | D. | 洪特规则特例 |
分析 泡利原理是指每个轨道最多只能容纳两个自旋相反的电子,能量最低原理是指核外电子优先排布能量最低的轨道,洪特规则是指在相同能量的轨道上,电子在排布的时候优先进入空轨道,每个轨道中的单电子取得相同自旋方向,洪特规则特例是指全充满、半充满、全空状态都是稳定状态.
解答 解:泡利原理是指每个轨道最多只能容纳两个自旋相反的电子,能量最低原理是指核外电子优先排布能量最低的轨道,洪特规则是指在相同能量的轨道上,电子在排布的时候优先进入空轨道,每个轨道中的单电子取得相同自旋方向,洪特规则特例是指全充满、半充满、全空状态都是稳定状态.np能级有3个轨道,根据泡利原理最多只能排布6个电子,而ns2np7的np能级排布了7个电子,故违背了泡利原理.故选:A.
点评 本题考查了原子核外电子的排布规律,注意泡利原理和洪特规则的概念的辨析,也注意相关基础知识的积累.


科目:高中化学 来源: 题型:选择题
| 实验编号 | c(HA)/mol•L-1 | c(NaOH)/mol•L-1 | 反应后溶液pH |
| 甲 | 0.1 | 0.1 | 9 |
| 乙 | c1 | 0.2 | 7 |
| A. | 甲:反应后溶液中 c(Na+)>c(A-)>c(OH-)>c(H+) | |
| B. | 乙:反应后溶液中 c(Na+)=c(HA)+c(A-) | |
| C. | 甲中由水电离产生的c(H+)=1×10-9 mol•L-1 | |
| D. | 乙中c1一定大于0.2 mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
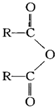 $\stackrel{H_{2}O}{→}$2RCOOH(其中R是烃基)
$\stackrel{H_{2}O}{→}$2RCOOH(其中R是烃基)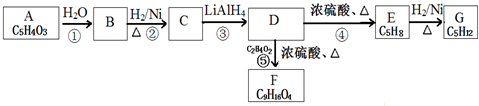
 ,CH2=C(CH3)CH=CH2.
,CH2=C(CH3)CH=CH2.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ③④ | C. | ②③ | D. | ②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 元素代号 | X | Y | Z | W |
| 原子半径/pm | 160 | 143 | 70 | 66 |
| 主要化合价 | +2 | +3 | +3、+5、-3 | -2 |
| A. | X、Y元素的金属性X<Y | |
| B. | Y的最高价氧化物对应的水化物能溶于稀氨水 | |
| C. | 一定条件下,W单质可以将Z从其氢化物中置换出来 | |
| D. | 常温下,Z单质与W的常见单质直接生成2W2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;
;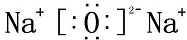 ;
; ;
; ;
; ;
;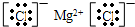 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化钙晶体中阴、阳离子所带电荷数多 | |
| B. | 氧化钙晶格能比氯化钠的晶格能大 | |
| C. | 两种晶体的晶胞结构类型不同 | |
| D. | 氧化钙、氯化钠的离子间距类似情况下,晶格能主要由阴、阳离子所带电荷数决定 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
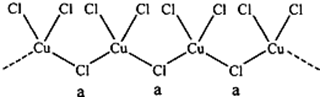
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 13C和14C属于同一种元素,它们互为同位素 | |
| B. | 1H和2H是不同的核素,它们的化学性质基本相同 | |
| C. | 14C和14N的质量数相等,它们的中子数不等 | |
| D. | 6Li和7Li的电子数相等,中子数也相等 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com