
20℃时,PbCl2(s)在不同浓度盐酸中的最大溶解量(单位:g/L)如右图所示。下列叙述正确的是
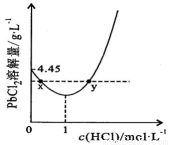
A.盐酸浓度越大,Ksp(PbCl2)越大
B.PbCl2能与一定浓度的盐酸反应
C.x、y两点对应的溶液中c(Pb2+)相等
D.往含Pb2+的溶液中加入过量浓盐酸,可将Pb2+完全转化为PbCl2(s)
科目:高中化学 来源:2016-2017学年四川省高二上半期考试化学卷(解析版) 题型:选择题
下列关于晶体的叙述中,不正确的是
A、金刚石网状结构中,由共价键形成的碳原子环其中最小环有6个碳原子
B、在氯化钠的晶体中,每个Na+或Cl-的周围都紧邻6个Cl-或Na+
C、在氯化铯晶体中,每个Cs+周围都紧邻8个Cl—,每个Cl—周围也紧邻8个Cs+
D、在干冰的晶体中,每个CO2分子周围都紧邻4个CO2分子
查看答案和解析>>
科目:高中化学 来源:2017届山东省东营市高三上期中化学卷(解析版) 题型:选择题
按下图所示装置进行实验,若x轴表示流入阴极的电子的物质的量,则y轴应表示( )
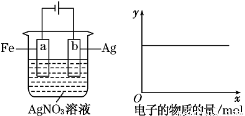
①c(Ag+) ②c(NO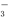 ) ③a棒的质量
) ③a棒的质量
④b棒的质量 ⑤c(H+)
A.①③ B.③④ C.①②④ D.①②⑤
查看答案和解析>>
科目:高中化学 来源:2017届山东省东营市高三上期中化学卷(解析版) 题型:选择题
下列离子方程式正确的是( )
A.用铜作电极电解饱和食盐水:2Cl-+2H2O 2OH-+Cl2↑+H2↑
2OH-+Cl2↑+H2↑
B.Fe3O4与过量的稀HNO3反应: Fe3O4+8H+ =Fe2++2Fe3++4H2O
C.向Ba(OH)2 溶液中逐滴加入NaHSO4溶液至Ba2+刚好沉淀完全:
Ba2++OH-+H++SO42-=BaSO4↓+H2O
D.NaHS溶液呈碱性:HS-+H2O  H3O++OH-+ S2-
H3O++OH-+ S2-
查看答案和解析>>
科目:高中化学 来源:2017届宁夏高三上学期统练三化学试卷(解析版) 题型:填空题
利用电化学原理可以解决很多问题。
(1)精确测量金属离子在惰性电极上以镀层形式沉积的金属质量,可以确定电解过程中通过电解池的电量。实际测量中常用的银电量计结构如图所示。

①电量计中的银棒应与电源的正极相连,铂坩埚上发生的电极反应是_____________;
②实验中,为了避免银溶解过程中可能产生的金属颗粒掉进铂埚而导致测量误差,常在银电极附近增加一个收集网袋。若没有收集网袋,测量结果会____________(填“偏高"“偏低”或“无影响”);
③若要测定电解精炼铜时通过的电量,可将该银电量计中的银棒与待测电解池的________电极相连。
(2)如图所示,将铁棒和石墨棒插人盛有饱和NaCl溶液的U型管中。
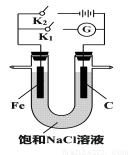
①K1闭合,铁棒上发生的反应为______________;
②K2闭合,铁棒不会被腐蚀,属于_________保护法。
查看答案和解析>>
科目:高中化学 来源:2017届宁夏高三上学期统练三化学试卷(解析版) 题型:选择题
常温下,向IL0.1mol/LNH4Cl溶液中,不断加入固体NaOH后,NH4+与NH3·H2O的变化趋势如右图所示(不考虑体积变化和氨的挥发),下列说法不正确的是

A.M点溶液中水的电离程度比原溶液小
B.在M点时,n(OH-)-n(H+)=(a-0.05)mol
C.随者NaOH的加入,c(H+)/c(NH4+)不断增大
D.当n(NaOH)=0.1mol时,c(OH-)>c(Cl-)-c(NH3·H20)
查看答案和解析>>
科目:高中化学 来源:2017届宁夏高三上学期统练三化学试卷(解析版) 题型:选择题
下列说法正确的是( )
A.常温下.NH4Cl溶液加水稀释,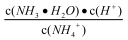 增大
增大
B.0.1mol/LNa2CO3溶液加热后,溶液的pH减小
C室温下稀释0.1mol/LCH3COOH溶液,溶液的导电能力减弱,因此溶液中所有离子浓度均减小
D.向沸水中滴加FeCl3饱和溶液制备Fe(OH)3胶体的原理是加热促进Fe3+水解
查看答案和解析>>
科目:高中化学 来源:2016-2017年吉林长春白城一中两校高二上期中化学卷(解析版) 题型:选择题
水解反应是一类重要的反应,下列物质不能水解的是
A.油脂 B.淀粉 C.蛋白质 D.果糖
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com