
��12�֣��ڻ�ѧ��Ӧ�У�ֻ�м�����������ƽ�������ߵö�ķ�Ӧ����ӷ�����ײʱ�ſ��ܷ�����ѧ��Ӧ����Щ���ӱ���Ϊ����ӡ�ʹ��ͨ���ӱ�ɻ���������ṩ������ȵ������л�ܣ��䵥λͨ����kJ��mol-1��ʾ��������۲���ͼ��Ȼ��ش����⡣
��1��ͼ����ʾ��Ӧ��_________(����ȡ����ȡ�)��Ӧ���÷�Ӧ_____________(���Ҫ������Ҫ��)���ȣ��÷�Ӧ�ġ�H =______________________(�ú�E1��E2�Ĵ���ʽ��ʾ)��
��2����֪�Ȼ�ѧ����ʽ��H2(g)�� O2(g) = 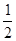 H2O(g)
��H =��241.8 kJ��mol-1���÷�Ӧ�Ļ��Ϊ167.2 kJ��mol-1�������淴Ӧ�Ļ��Ϊ____________________��
H2O(g)
��H =��241.8 kJ��mol-1���÷�Ӧ�Ļ��Ϊ167.2 kJ��mol-1�������淴Ӧ�Ļ��Ϊ____________________��
 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ��ӦC��s��+H2O��g��?CO��g��+H2��g����һ�ݻ��ɱ���ܱ������н��У��Իش�
��ӦC��s��+H2O��g��?CO��g��+H2��g����һ�ݻ��ɱ���ܱ������н��У��Իش�| 1 | 2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 �ڻ�ѧ��Ӧ�У�ֻ�м�����������ƽ�������ߵö�ķ�Ӧ����ӷ�����ײʱ���ܷ�����ѧ��Ӧ����������ѧ��Ӧ����ײ��֮Ϊ��Ч��ײ����Щ���ӳ�Ϊ����ӣ�ʹ��ͨ���ӱ�ɻ���������ṩ������ȵ������л�ܣ��䵥λ��kJ?mol-1��ʾ��������۲���ͼ��Ȼ��ش����⣮
�ڻ�ѧ��Ӧ�У�ֻ�м�����������ƽ�������ߵö�ķ�Ӧ����ӷ�����ײʱ���ܷ�����ѧ��Ӧ����������ѧ��Ӧ����ײ��֮Ϊ��Ч��ײ����Щ���ӳ�Ϊ����ӣ�ʹ��ͨ���ӱ�ɻ���������ṩ������ȵ������л�ܣ��䵥λ��kJ?mol-1��ʾ��������۲���ͼ��Ȼ��ش����⣮| 1 | 2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
��8�֣��ڻ�ѧ��Ӧ�У�ֻ�м�����������ƽ�������ߵö�ķ�Ӧ����ӷ�����ײʱ�ſ��ܷ�����ѧ��Ӧ����Щ���ӳ�Ϊ����ӣ�ʹ��ͨ���ӱ�ɻ���������ṩ������ȵ������л�ܣ��䵥λͨ����kJ/mol��ʾ��������۲���ͼ��Ȼ��ش����⣺
��1��ͼ����ʾ��Ӧ��_____________������ȡ����ȡ�����Ӧ���÷�Ӧ�ġ�H��____________���ú�E1��E2�Ĵ���ʽ��ʾ����
��2����֪�Ȼ�ѧ����ʽ��H2(g)��1/2O2(g)��H2O(g) ��H����241.8kJ��mol-1���÷�Ӧ�Ļ��Ϊ167.2kJ��mol-1�������淴Ӧ�Ļ��Ϊ ��
��3������ͬһ��Ӧ��ͼ�����ߣ�����ʵ�ߣ�����ȣ���ܴ�ͣ�����ӵİٷ������࣬��Ӧ�������Լӿ죬����Ϊ����ܵ�ԭ����
��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�ڻ�ѧ��Ӧ�У�ֻ�м�����������ƽ�������ߵö�ķ�Ӧ����ӷ�����ײʱ�ſ��ܷ�����ѧ��Ӧ����Щ���ӳ�Ϊ����ӣ�ʹ��ͨ���ӱ�ɻ���������ṩ������ȵ������л�ܣ��䵥λͨ����kJ/mol��ʾ��������۲���ͼ��Ȼ��ش����⡣
��1��ͼ����ʾ��Ӧ��_________������ȡ����ȡ�����Ӧ���÷�Ӧ________�����Ҫ������Ҫ�������ȣ��÷�Ӧ�ġ�H��___________________kJ/mol���ú�E1��E2�Ĵ���ʽ��ʾ����
��2����֪�Ȼ�ѧ����ʽ��H2��g���� 0.5 O2��g����H2O��g������H����241.8 kJ��mol
�÷�Ӧ�Ļ��Ϊ167.2kJ��mol�������淴Ӧ�Ļ��Ϊ____________________��
��3������ͬһ��Ӧ��ͼ�����ߣ�����ʵ�ߣ�����ȣ���ܴ�ͣ�����ӵİٷ������࣬��Ӧ���ʼӿ죬����Ϊ����ܵ�ԭ���ǣ�___________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011-2012ѧ�꺣��ʡ������ѧ�߶���ѧ����ĩ���Ի�ѧ�Ծ����������� ���ͣ������
�ڻ�ѧ��Ӧ�У�ֻ�м�����������ƽ�������ߵö�ķ�Ӧ����ӷ�����ײʱ���ܷ�����ѧ��Ӧ����������ѧ��Ӧ����ײ��֮Ϊ��Ч��ײ����Щ���ӳ�Ϊ����ӡ�ʹ��ͨ���ӱ�ɻ���������ṩ������ȵ������л�ܣ��䵥λ��kJ?mol-1��ʾ��������۲���ͼ��Ȼ��ش����⡣
��1��ͼ�з�Ӧ�� ������ȡ����ȡ�����Ӧ���÷�Ӧ �����Ҫ������Ҫ�����ṩ�������÷�Ӧ�ġ�H= ���ú�E1��E2�Ĵ���ʽ��ʾ����
��2����֪�Ȼ�ѧ����ʽ��H2(g)+1/2O2(g) === H2O(g) ��H=��241.8kJ?mol-1���÷�Ӧ�Ļ��Ϊ167.2 kJ?mol-1�������淴Ӧ�Ļ��Ϊ ��
��3������ͬһ��Ӧ��ͼ������(II)��ʵ��(I)��ȣ���ܴ�ͣ�����ӵİٷ������࣬��Ӧ���ʼӿ죬����Ϊ����ܵ�ԭ���� ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com