
| A. | 质量数 | B. | 中子数 | C. | 质子数 | D. | 电子数 |
 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案 一卷搞定系列答案
一卷搞定系列答案 名校作业本系列答案
名校作业本系列答案 轻巧夺冠周测月考直通名校系列答案
轻巧夺冠周测月考直通名校系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离平衡常数(25℃) | Ki=1.77×10-4 | Ki=5.0×10-10 | Ki1=4.3×10-7 Ki2=5.6×10-11 |
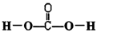 .
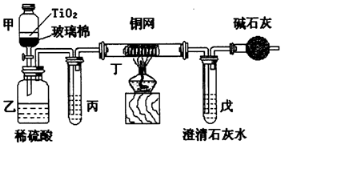
.
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 两者都能溶于水并且都能和水反应,前者的溶解度大于后者 | |
| B. | 两者都能用于治疗胃酸过多疾病,前者的效果好于后者 | |
| C. | 足量的Na2CO3和NaHCO3分别与等物质的量的稀盐酸反应,前者产生CO2多 | |
| D. | 等体积等浓度的AlCl3溶液分别和足量的Na2CO3和NaHCO3反应,前者产生CO2多 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
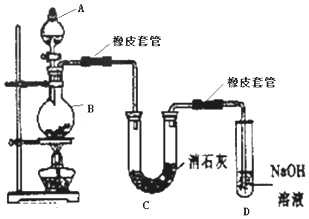
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 钠燃烧,可用砂子灭火,不能用二氧化碳灭火器来灭火 | |
| B. | 眼睛里不慎溅进了稀药液,应立即用水冲洗,并且用手使劲揉眼睛 | |
| C. | 少量浓硫酸沾到皮肤上,立即用氢氧化钠溶液冲洗 | |
| D. | 熄灭酒精灯可直接用嘴吹 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | +2 | B. | +3 | C. | +4 | D. | +5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | C | |
| B |
| A. | B为第二周期的元素 | B. | C为第五主族元素 | ||
| C. | A的原子序数为6 | D. | C是非金属性最强的元素 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com