
在一定温度下,可逆反应A(g)+3B(g)  2C(g)达到平衡的标志是
2C(g)达到平衡的标志是
A. A的生成速率与C分解的速率相等
B.单位时间生成n mol A的同时生成3n mol B
C. A .B.C的浓度不再变化
D. A .B.C的分子个数之比为1:3:2
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案科目:高中化学 来源:2015-2016学年广东省高一下期中化学试卷(解析版) 题型:选择题
以锌片和铜片为电极,以稀硫酸为电解质溶液的原电池中,当导线中通过2mol电子时,下列说法正确的是
A.锌片溶解了1mol,铜片上析出1mol氢气 B.锌片发生还原反应
C.正极附近的SO42-离子浓度逐渐增大 D.电池工作时,电子由正极通过外电路流向负极
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广西河池高中高一下第二次月考化学试卷(解析版) 题型:实验题
某同学在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。请回答下列问题:
(1)硫酸铜溶液可以加快氢气生成速率的原因是_________;
(2)实验室中现有Na2SO4、MgSO4、HgSO4、K2SO4等4种溶液,可与实验中CuSO4溶液起相似作用的是__________;
(3)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验。将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需时间。
实验 混合溶液 | A | B | C | D | E | F |
4mol·L-1H2SO4溶液/mL | 30 | V1 | V2 | V3 | V4 | V5 |
饱和CuSO4溶液/mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
H2O/mL | V7 | V8 | V9 | V10 | 10 | 0 |
①请完成此实验设计,其中:V1=______mL,V9=_____mL;
②该同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高,但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因_____________________________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广西河池高中高一下第二次月考化学试卷(解析版) 题型:选择题
张清莲是我国著名的化学家,1991年,他准确测得In的原子量为114.818,被国际原子量委员会采用为新的标准值。这是原子量表中的首次采用我国测定的原子量值。己知In的原子核外电子由里到外排布为2, 8, 18, 18, 3。则下列关于In的说法不正确的是( )
A.In为过渡元素 B.In为长周期元素
C.In易导电导热 D.In 在反应中容易失电子
查看答案和解析>>
科目:高中化学 来源:2015-2016学年云南省高一下期中化学试卷(解析版) 题型:选择题
足量铜溶于一定量浓硝酸,产生NO2、N2O4、NO的混合气体,这些气体若与2.24LO2(标准状况)混合后通入水中,气体被水完全吸收。若向原所得溶液中加入l0mol·L-1H2SO4溶液100mL,则继续溶解的Cu的质量为
A.0 B.32g C.38.4g D.48g
查看答案和解析>>
科目:高中化学 来源:2015-2016学年云南省高一下期中化学试卷(解析版) 题型:选择题
通过对实验现象的观察、分析推理得出正确的结论是化学学习的方法之一。对下列实验事实的解释正确的是
现象或操作 | 解 释 | |
A | KI淀粉溶液中通入Cl2,溶液变蓝 | Cl2能与淀粉发生显色反应 |
B | 浓HNO3在光照条件下变黄 | 浓HNO3不稳定,生成有色产物能溶于浓硝酸 |
C | 某溶液中加入硝酸酸化的氯化钡溶液,有白色沉淀生成 | 说明该溶液中含有SO42- |
D | 铜片放入浓硫酸中,无明显变化 | 说明铜在冷的浓硫酸中发生钝化 |
查看答案和解析>>
科目:高中化学 来源:2015-2016学年云南省高一下期中化学试卷(解析版) 题型:选择题
2SO2(g)+O2(g) 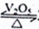 2SO3(g)是制备硫酸的重要反应。下列叙述正确的是
2SO3(g)是制备硫酸的重要反应。下列叙述正确的是
A.催化剂V2O5不改变该反应的逆反应速率
B.恒压,通入稀有气体,反应速率不变
C.该反应是放热反应,降低温度将缩短反应达到平衡的时间
D.在t1、t2时刻,SO3(g)的浓度分别是C1mol/L,C2 mol/L,则时间间隔t1(s)~t2(s)内,SO3(g)消耗的平均速率为 V=(C2-C1)/(t2-t1) mol/(L·s)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高二下期中化学试卷(解析版) 题型:选择题
氯在饮用水处理中常用作杀菌剂,且HClO的杀菌能力比ClO-强。25℃时氯气-氯水体系中存在以下平衡关系:
Cl2(g)  Cl2(aq) K1=10-1.2
Cl2(aq) K1=10-1.2
Cl2(aq)+ H2O  HClO + H+ +Cl- K2=10-3.4
HClO + H+ +Cl- K2=10-3.4
HClO  H+ + ClO- Ka=?
H+ + ClO- Ka=?
其中,Cl2(aq)、HClO和ClO-分别在三者中所占分数(α)随pH变化的关系如图所示。下列表述正确的是
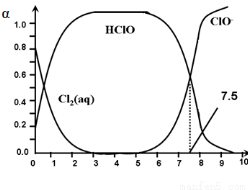
A.氯处理饮用水时,在夏季的杀菌效果比在冬季好
B.用氯处理饮用水时,pH=7.5时杀菌效果比pH=6.5时好
C.在氯处理水体系中,c(HClO) +c(ClO-) =c(H+)-c(OH-)
D.Cl2(g)+ H2O  2H+ + ClO- + Cl- ,K=10-12.1
2H+ + ClO- + Cl- ,K=10-12.1
查看答案和解析>>
科目:高中化学 来源:2016届吉林省高三第五次模拟理综化学试卷(解析版) 题型:填空题
二十一世纪钛将成为铁、铝之后的第三大金属,工业上以钛铁矿为原料制备二氧化钛及钛的工艺流程如下图所示,钛铁矿的主要成分为钛酸亚铁(FeTiO3),其中一部分铁元素在风化过程中会转化为+3价,FeTiO3溶于酸后Ti元素以TiO2+存在,TiOSO4遇水可水解。
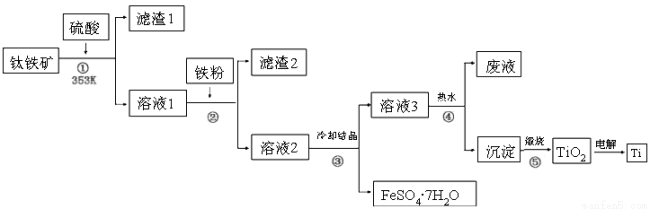
请根据以上信息回答下列问题:
(1)②中加入铁粉的目的是__________;
(2)③中混合物分离的依据是________(填字母序号)。
a.熔、沸点差异 b.溶解性差异 c.氧化性、还原性差异
(3)②、③、④中均需要进行的操作是________(填操作名称)。
(4)写出④的离子方程式:_______________;该过程在热水中操作的目的是_________
(5)利用生产过程中的废液与软锰矿(主要成分为MnO2)反应可生产硫酸锰(MnSO4,易溶于水),该反应的离子方程式为_______________。
(6)科学家从电解冶炼铝的工艺得到启发.找出了冶炼钛的新工艺。
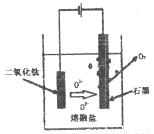
①直接电解固体TiO2法生产钛,原理如图所示,则阴极获得钛的电极反应为_____________。
②电解一段时间后,需要更换石墨电极,原因是_____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com