
| A、用CCl4萃取溴水中的溴,可观察到溶液分层,上层为橙红色,下层接近无色 |
| B、石油的裂化、煤的液化和煤的气化都属于化学变化 |
| C、热的苯酚浓溶液放入冷水中冷却,溶液变浑浊,此时发生了化学反应 |
| D、往蛋白质溶液里加入饱和的CuSO4溶液,可提纯蛋白质 |


科目:高中化学 来源: 题型:
| A、福尔马林能使蛋白质变性 |
| B、臭氧的氧化性极强,可用于饮用水的消毒 |
| C、氧化镁的熔点很高,可用于制造耐火材料 |
| D、钠、钾合金常温下呈液态,可用于快中子反应堆的热交换剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 混合物 | 试剂 | 分离方法 | |
| A | 苯(苯酚) | 溴水 | 过滤 |
| B | 乙烷(乙烯) | 酸性高锰酸钾 | 洗气 |
| C | 硬脂酸钠(甘油、水) | 氯化钠粉末 | 分液 |
| D | 福尔马林(蚁酸) | 饱和Na2CO3溶液 | 蒸馏 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、平衡时,N2的物质的量是3.6mol |
| B、平衡时,H2的物质的量是10.8mol |
| C、平衡时,N2的转化率为10% |
| D、NH3的体积百分含量是10% |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、丁硫醇、甲硫醇与乙硫醇互为同系物 |
| B、沸点不同的丁硫醇有三种 |
| C、从结构上分析了巯基(-SH)上的氢原子比羟基(-OH)上的氢原子难电离 |
| D、与乙醇相似,乙硫醇分子间存在氢键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
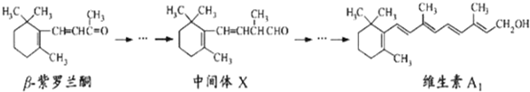
| A、维生素A1难溶于水,也难溶于NaOH溶液 |
| B、β-紫罗兰酮与中间体X互为同系物 |
| C、1molβ-紫罗兰酮与1molCl2发生加成反应可得到3种不同产物 |
| D、β-紫罗兰酮能发生加成反应、取代反应、氧化反应、还原反应、加聚反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 溶质 | AgNO3 | Ba(NO3)2 | AgCl | BaCl2 |
| 溶剂 | ||||
| 水 | 170 | 9.2 | 1.5×10-4 | 33.3 |
| 液氨 | 86 | 97.2 | 0.8 | 0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加水时,平衡向逆向移动 |
| B、加入少量固NaOH体,平衡向正向移动 |
| C、加入少量0.1mol/L盐酸,溶液c(H+)减小 |
| D、加入少量CH3COONa固体,平衡向正向移动 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com