
【题目】某0.2L无土栽培用的营养液中含有KCl、K2SO4、NH4Cl三种溶质,测得该营养液中部分离子的浓度柱状图如图甲所示:

(1)该营养液中K2SO4的物质的量浓度为____mol·L-1,含KCl的质量为____。
(2)该营养液中NH4Cl的物质的量为____。
(3)将该营养液加水稀释,稀释过程中NH![]() 的浓度(c)随溶液体积(V)变化的曲线如图乙所示,则V1=____,V2=___。
的浓度(c)随溶液体积(V)变化的曲线如图乙所示,则V1=____,V2=___。
【答案】4.0 14.9g 1.6mol 0.2 1.0
【解析】
(1)根据硫酸根离子的浓度可知硫酸钾的物质的量浓度,根据钾离子守恒可以计算出氯化钾的浓度及质量;
(2)根据氯离子的总浓度、氯化钾的浓度可以计算出氯化铵的物质的量浓度,再根据n=cV计算出氯化铵的物质的量;
(3)据c=n/V可知V=n/c,代入数据求算即可。
(1)硫酸根离子物质的量浓度为4.0mol·L-1,则硫酸钾的物质的量浓度为:c(K2SO4)=c(SO42-)=4.0mol·L-1;根据钾离子守恒可知,c(K+)=c(KCl)+2c(K2SO4),则c(KCl)=c(K+)-2c(K2SO4)=9.0mol·L-1-4.0mol·L-1×2=1.0mol·L-1,溶质氯化钾的质量为:m(KCl)=McV=74.5g·mol-1×1.0mol·L-1×0.2L=14.9 g;
(2)根据氯原子守恒可知,c(Cl-)=c(KCl)+c(NH4Cl),则:c(NH4Cl)=c(Cl-)-c(KCl)=9.0mol·L-1-1.0mol·L-1=8.0mol·L-1,氯化铵的物质的量为:n(NH4Cl)=8.0mol·L-1×0.2L=1.6mol;
(3)据c=n/V可知V=n/c,V1=1.6mol/8mol·L-1=0.2L,V2=1.6mol/1.6mol·L-1=1.0L;


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列与阿伏加德罗常数的值(NA)有关的说法中,不正确的是
A. 18g H218O与D2O的混合物中,中子数为9NA
B. 标准状况下,22.4 L Cl2与NaOH溶液完全反应时转移电子的数为NA
C. 1L0.1 mol L-1NH4NO3溶液中加稀氨水,溶液呈中性时NH![]() 数为0.1NA
数为0.1NA
D. 4.6 gC2H6O中含有的C—H数目为0.6NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用容量瓶配制一定物质的量浓度的NaCl溶液的实验中,会使所配溶液浓度偏高的是
A. 称量NaCl固体时砝码上有杂质
B. 没有洗涤溶解NaCl固体的烧杯和玻璃棒
C. 定容时加水加多了,用滴管吸出溶液至刻度线
D. 定容时仰视刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为除去粗盐中的CaCl2、MgCl2、硫酸盐以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下:
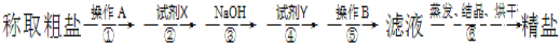
(1)第①步中,操作A是__________,第⑤步中,操作B是__________。
(2)判断试剂X过量的方法是________________________。
(3)写出第④步中涉及反应的化学方程式____________________。
(4)第⑤步操作中得到的固体成分有:泥沙、CaCO3、Mg(OH)2、__________(填化学式)。
(5)此实验方案尚需完善,具体步骤是__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中华传统文化蕴含着很多科学知识,下列说法错误的是
A. “丹砂(HgS烧之成水银,积变又还成丹砂”描述的是可逆反应
B. “水声冰下咽,沙路雪中平”未涉及化学变化
C. “霾尘积聚难见路人”形容的霾尘中有气溶胶,具有丁达尔效应
D. “含浆似注甘露钵,好与文园止消渴”说明柑橘糖浆有甜味,可以止渴
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】0.1mol/LCH3COOH溶液加水稀释或升高温度的过程中,下列表达式的数值一定变大的是
A. c(H+) B. c(H+)·c(OH-) C. ![]() D.
D. ![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种正投入生产的大型蓄电系统如图所示。放电前,被交换膜隔开的电解质为Na2S2和NaBr3,放电后分别变为Na2S4和NaBr。下列叙述不正确的是

A. 放电时,负极的电极反应式为2S22――2e-===S42-
B. 充电时,阳极的电极反应式为3Br--2e-===Br3-
C. 放电时,Na+经过离子交换膜,由b池移向a池
D. 充电时,M接电源负极,N接电源正极
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是
A.将纯水加热的过程中,Kw变大,pH变小
B.保存FeSO4溶液时,加入稀HNO3抑制Fe2+水解
C.FeCl3溶液蒸干、灼烧至恒重,最终得到FeCl3固体
D.向0.1 molL-1氨水中加入少量水,pH减小,![]() 减小
减小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com