
| A.对于反应nA(g)+B(g)?2C(g),平衡后增大压强,A的百分含量减小,则n≥2 |
| B.对于反应2A(g)?B(g)△H<0,若体系温度不再变化说明反应达到平衡状态 |
| C.对于反应2A(g)?B(g),恒温,恒容条件下气体密度不再变化,说明反应达到平衡状态 |
| D.对于反应2A(g)?B(g),若v(A)正=2v(B)逆,说明反应达到平衡状态 |
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.有1molH-H键断裂,同时有1molI-I键形成 |
| B.容器内压强不再随时间而变化 |
| C.单位时间内反应掉nmolI2同时生成2nmolHI |
| D.H2、I2、HI的浓度之比为1:1:2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.混合气体的压强 | B.混合气体的密度 |
| C.C、D的物质的量的比值 | D.气体的总物质的量 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题

查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
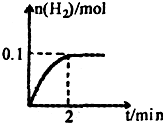
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 压强\A转化率\温度 | p1(MPa) | p2(MPa) |
| 400℃ | 99.6 | 99.7 |
| 500℃ | 96.9 | 97.8 |
A.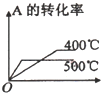 | B.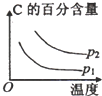 | C.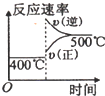 | D.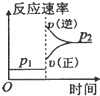 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.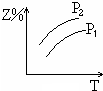 | B.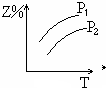 | C.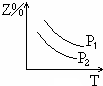 | D.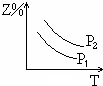 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com