
| A、加入Al能放出H2的溶液中:Cl-、SO42-、NO3-、Mg2+ |
| B、能使淀粉碘化钾试纸显蓝色的溶液中:K+、SO42-、S2-、SO32- |
| C、c(H+):c(OH-)=1:1012的水溶液中:CO32-、Na+、NO3-、AlO2- |
| D、无色溶液中:K+、Na+、MnO4-、SO42- |


 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案 ABC考王全优卷系列答案
ABC考王全优卷系列答案科目:高中化学 来源: 题型:
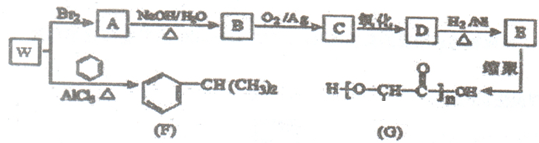
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①③⑤ | B、②④ |
| C、①③④⑤ | D、①②③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、由水电离的c(H+)=10-12mol?L-1的溶液中:Cl-、CO32-、K+、SO32- |
| B、含有大量AlO2-的溶液中:K+、Al3+、Br-、HCO3- |
| C、1.0mol?L-1的KNO3溶液:H+、Fe2+、Cl-、SO42- |
| D、使pH试纸变深蓝色的溶液中:Cl-、K+、Mg2+、SO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,22.4L的CCl4中含有的分子数为NA |
| B、18gD2O中含有的电子数为NA |
| C、1L1 mol/L的盐酸溶液所含的分子数为NA |
| D、4 g氦气中所含的质子数为2 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
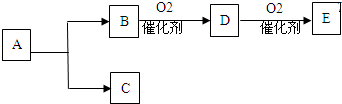
查看答案和解析>>
科目:高中化学 来源: 题型:
| 平行实验编号 | Na2C2O4质量 (m g) | 滴定管起始读数(mL) | 滴定管滴定终点读数(mL) |
| 1 | 1.34 | 0.00 | 25.02 |
| 2 | 1.34 | 0.02 | 25.00 |
| 3 | 1.34 | 0.18 | 25.18 |
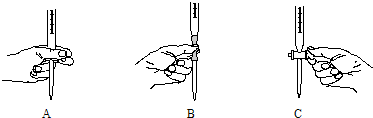
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com