
| A. | 30℃ | B. | 40℃ | C. | 50℃ | D. | 60℃ |
 智慧课堂密卷100分单元过关检测系列答案
智慧课堂密卷100分单元过关检测系列答案 单元期中期末卷系列答案
单元期中期末卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 羰基硫中O为-2价,C、S都是+1价 | |
| B. | 羰基硫分子中共含有3个原子核、16个电子 | |
| C. | 羰基硫分子结构中只含有极性共价键 | |
| D. | 羰基硫的电子式为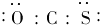 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{M}{10s•ρ}$mol/L | B. | $\frac{1000s•ρ}{M(100+s)}$mol/L | ||
| C. | $\frac{10s•ρ}{M}$mol/L | D. | $\frac{M(100+s)}{1000s•ρ}$mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
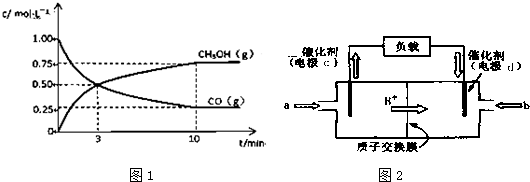
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
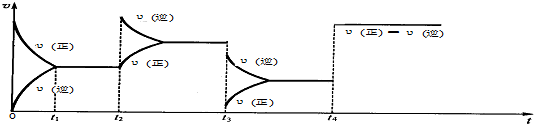
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
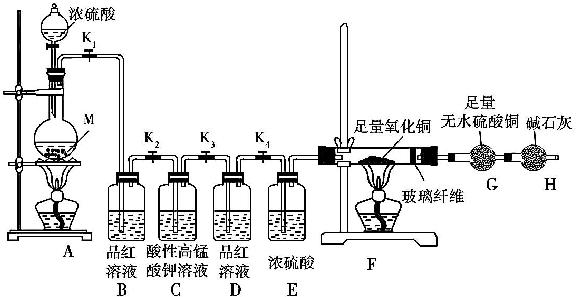
| 装置 | B | F | G |
| 实验现象 | |||
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 陈述I | 陈述Ⅱ | 判断 |
| A | 铜绿的主要成分是碱式碳酸铜 | 可用稀盐酸除铜器表面的铜绿 | Ⅰ对;Ⅱ对 无 |
| B | 铜绿的主要成分是碱式碳酸铜 | 铜制容器可以盛放浓硫酸 | I对;Ⅱ对;有 |
| C | 向硫酸铜溶液通足量氨气.有深蓝色沉淀产生,过滤后灼烧滤渣,最后变成黑色固体 | 把铜丝放在酒楕灯火焰上灼烧铜丝表面变黑 | I对;Ⅱ对;有 |
| D | 蓝色硫酸铜晶体受热转化为白色硫酸铜粉末是物理变化 | 硫酸铜溶液可用作游泳池的消毒剂 | 错;Ⅱ对;无 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验 | 反应温度/℃ | Na2S2O3溶液 | 稀H2SO4 | H2O | ||
| V/mL | c/(mol•L-1) | V/mL | c/(mol•L-1) | V/mL | ||
| A | 25 | 5 | 0.1 | 10 | 0.1 | 5 |
| B | 25 | 5 | 0.2 | 5 | 0.2 | 10 |
| C | 35 | 5 | 0.1 | 10 | 0.1 | 5 |
| D | 35 | 5 | 0.2 | 5 | 0.2 | 10 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com