
【题目】在25℃的纯水中通入一定量的氯化氢,当溶液的pH=1时,则由水电离出的c(H+)是( )
A.1×10﹣1mol/L
B.1×10﹣6mol/L
C.1×10﹣3mol/L
D.1×10﹣13mol/L
科目:高中化学 来源: 题型:
【题目】向含有MgCO3固体的溶液中滴加少许浓盐酸(忽略体积变化),下列数值变小的是( )
A.c(CO32﹣)
B.c(Mg2+)
C.c(H+)
D.Ksp(MgCO3)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】若NA表示阿伏加德罗常数的值,下列叙述中正确的是( )
A. 1mol Cl2参加化学反应,转移的电子数一定为2NA
B. 7.8g Na2O2 晶体中阴阳离子总数为0.4NA
C. 15.6 g Na2O2与过量CO2反应时,转移的电子数为0.2NA
D. 标准状况下,由0.5mol NO和0.5mol O2组成的混合气体,分子数约为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸是中学化学实验室的常见药品,回答下列问题:
I.配制一定物质的量浓度的硫酸溶液:
(1)某次实验大约需要1mol/L硫酸溶液435mL。同学们发现实验室内没有450mL的容量瓶,某同学提议用1个200mL容量瓶和1个250mL容量瓶来配制,你认为该提议______(填“合理”、“不合理”)。
(2)实验中要配制0.5mol/L H2SO4溶液250mL,则需量取密度为1.84g/mL、98%的浓硫酸________mL(结果保留小数点后一位)。
Ⅱ.蔗糖与浓硫酸的炭化实验会产生大量的有刺激性气味的气体,会对环境造成污染。 某实验小组利用如下装置对该实验进行改进。回答下列问题:

注:硬质玻璃管中①、②、③处分别为滴有Na2S溶液的滤纸、滴有品红溶液的滤纸、滴有酸性KMnO4溶液的滤纸,a和b分别为两个小气球。
(3)实验开始后先关闭活塞K,硬质玻璃管中①号试纸变黄,②号和③号滤纸均褪色,a处气球变大。硬质玻璃管中实验现象说明炭化实验产生的刺激性气味气体是 SO2,
①、②、③处发生的变化分别说明SO2具有_______、________和__________(填SO2表现出的性质)。
(4)SO2和Cl2均可以使品红溶液褪色,但将两种气体按体积比1:1混合通入品红溶液中,品红溶液不褪色,其原因是___________(用化学方程式回答)。
(5)打开活塞K, a处气球变小,b处气球变大。使三颈烧瓶内气体缓慢通过B瓶和C瓶,一段时间之后,发现澄清石灰水变浑浊。为证明有CO2生成,可以在④号位罝的滤纸滴加_______溶液,该试剂的作用是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ClO2是一种国际上公认的安全无毒的绿色水处理剂。回答下列问题:
(1)工业废水的处理:某实验兴趣小组通过下图装置,利用稀硫酸、KClO3和草酸溶液制备ClO2,并用它来处理含Mn2+的工业废水。

①A装置的名称是______________,C装置的作用为__________________。
②B中反应产物有ClO2、CO2等,请写出该反应的化学方程式:___________________。
③写出装置D中除去Mn2+的离子方程式__________________。(已知Mn2+转化为MnO2)
(2)ClO2易溶于水。用水吸收ClO2得到ClO2溶液。为测定所得溶液中ClO2的含量,进行了下列实验:
步骤1:准确量取ClO2溶液10.00mL,稀释成100.00mL试样:量取V1mL试样加入到锥形瓶中;
步骤2:调节试样的pH≤2.0,加入足量的KI晶体,静置片刻;
步骤3:加入淀粉指示剂,用cmol·L-1Na2SO3溶液滴定至终点,消耗Na2S2O3溶液V2mL。 (已知2Na2S2O3+I2=Na2S4O6+2NaI)
①滴定终点的判断依据是___________________。
②原ClO2溶液的浓度为_______________g/L(用步骤中的字母代数式表示)。
③若实验中使用的Na2S2O3标准溶液部分因被氧气氧化而变质,则实验结果___________(填“偏高”、“ 偏低”或“无影响”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应4A(g)+5B(g)4C(g)+6D(g) 在5L的密闭容器中进行反应,30min后,C的物质的量增加了0.30mol.下列叙述正确的是( )
A.30min中A的平均反应速率是0.010molL﹣1min﹣1
B.容器中D的物质的量一定增加了0.45mol
C.容器中A,B,C,D的物质的量的比一定是4:5:4:6
D.容器中A的物质的量一定增加0.30mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在某100mL混合溶液中,硝酸和硫酸的物质的量浓度分别为0.4mol/L和0.1mol/L,向该混合溶液中加入1.92克铜粉,加热待充分反应后,所得溶液中的Cu2+的物质的量浓度是________________ mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将2.5gNaHCO3、Na2CO3、NaOH的固体混合物完全溶解于水,制成溶液,然后向该溶液中逐滴加入1mol/L的盐酸,所加盐酸的体积与产生CO2的体积(标准状况)关系如图所示,下列说法中错误的是
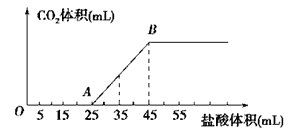
A. OA段发生反应的离子方程式为:OH-+H+==H2O H++CO32-==HCO3-
B. 当加入35mL盐酸时,产生CO2的体积为336mL
C. 混合物中NaOH的质量0.6g
D. A点溶液中的溶质为NaCl、NaHCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国政府为了消除碘缺乏病,规定在食盐中必须加入适量的碘酸钾。检验食盐中是否加碘,可利用如下反应:
KIO3+ KI+ H2SO4═ K2SO4+ I2 + H2O
(1)配平该方程式,并且用双线桥法表示该方程式电子转移的方向与数目:____________________
(2)该反应中氧化剂和还原剂的物质的量之比为______________;
(3)如果反应中转移0.5mol电子,则生成I2的物质的量为____________;
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com