
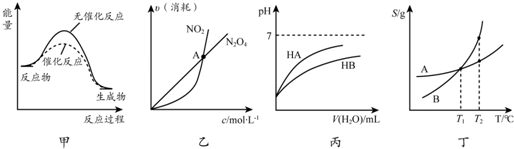
| A. | 由甲可知:使用催化剂不影响反应热 | |
| B. | 由乙可知:对于恒温恒容条件下的反应2NO2(g)?N2O4(g),A点为平衡状态 | |
| C. | 由丙可知:同温度、同浓度的NaA溶液与NaB溶液相比,其pH前者小于后者 | |
| D. | 由丁可知:将T1℃的A、B饱和溶液升温至T2℃时,A与B溶液的质量分数相等 |
分析 A.催化剂改变反应速率不改变化学平衡,反应热不变;
B.化学方程式可知二氧化氮和四氧化二氮反应速率之比等于星峰传说计量数之比为2:1,化学平衡状态需要正逆反应速率相同;
C.加入水稀释相同倍数,HA酸溶液PH增大的多,说明HA酸性大于HB,酸越弱对应盐水解程度越大,碱性越强;
D.将T1℃的A、B饱和溶液升温至T2℃时,溶液中溶质溶解度增大,变为不饱和溶液,
解答 解:A.催化剂能降低反应的活化能,加快反应速率化学平衡不变,反应的反应热不变,故A正确;
B.对于恒温恒容条件下的反应2NO2(g)?N2O4(g),图象中的A点是二氧化氮和四氧化二氮的消耗速率相同,但不能说明正逆反应速率相同,只有二氧化氮消耗速率为四氧化二氮消耗速率的二倍时才能说明反应达到平衡状态,故B错误;
C.图象分析可知加入水稀释相同倍数,HA酸溶液PH增大的多,说明HA酸性大于HB,酸越弱对应盐水解程度越大,碱性越强,所以同温度、同浓度的NaA溶液与NaB溶液相比,其pH前者小于后者,故C正确;
D.将T1℃的A、B饱和溶液升温至T2℃时,溶液中溶质溶解度增大,变为不饱和溶液,但溶液浓度和T1点的饱和溶液溶质质量分数相同,故D正确;
故选B.
点评 本题考查了图象变化实质的分析判断,主要是化学平衡影响因素、盐类水解原理、弱电解质电离平衡的影响因素、溶质质量分数的分析判断等知识,题目难度中等.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | Na+、Mg2+、Cl-、CO32- | B. | H+、Na+、Fe2+、NO3- | ||
| C. | K+、Ca2+、Cl-、NO3- | D. | K+、NH4+、OH-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
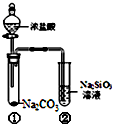
| A. | 向Na2SiO3溶液中直接滴入盐酸溶液无明显现象 | |
| B. | 试管①中反应的离子方程式是:Na2CO3+2H+═2Na++CO2↑+H2O | |
| C. | 该实验可以证明酸性:盐酸>碳酸>硅酸 | |
| D. | 一段时间后试管②中有胶冻状物质生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
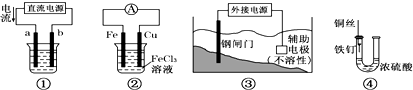
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 气体A的平衡转化率大于气体B平衡转化率 | |
| B. | 平衡后若减小该体系的压强,则平衡向左移动,化学平衡常数减小 | |
| C. | 物质D的聚集状态一定是气体 | |
| D. | 平衡后升高温度,若平衡向左移动,则正反应的△H>0 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该混合液中一定含有:K+、NH4+、CO32-、SO42-,可能含Cl- | |
| B. | 该混合液中一定含有:NH4+、CO32-、SO42-,可能含K+、Cl- | |
| C. | 该混合液中一定含有:NH4+、CO32-、SO42-,可能含Mg2+、K+、Cl- | |
| D. | 该混合液中一定含有:NH4+、SO42-,可能含Mg2+、K+、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 充电时,电池的阳极反应为LiC6-e=Li++C6 | |
| B. | 放电时,电池的正极反应为 CoO2+Li++e-=LiCoO2 | |
| C. | 乙酸、乙醇等含活泼氢的有机物可做该锂离子电池的电解质 | |
| D. | 该锂离子电池的比能量(消耗单位质量电极所释放的电量)比铅蓄电池低 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com