
A.一定条件下,混合气体的平均相对分子质量不再改变,表明已达平衡状态
B.一定条件下,H2O的生成速率与CO的消耗速率相等,表明已达平衡状态
C.增大水蒸气的浓度可提高CO的转化率
D.增大CO的浓度可提高CO的转化率
 全能测控期末小状元系列答案
全能测控期末小状元系列答案科目:高中化学 来源: 题型:阅读理解

| ||
| 1 |
| 2 |
| 1 |
| 2 |
| 化学键 | C-C | C-H | H-H | S-H | S-S | S-C |
| 键能/kJ.mol-1 | a | b | c | d | e | f |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
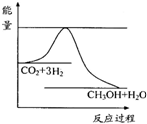 (2009?徐州二模)煤化工是以煤为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业过程.
(2009?徐州二模)煤化工是以煤为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业过程.| 实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | ||
| H2O | CO | H2 | CO | |||
| 1 | 650 | 2 | 4 | 1.6 | 2.4 | 5 |
| 2 | 900 | 1 | 2 | 0.4 | 1.6 | 3 |
| 3 | 900 | a | b | c | d | t |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:学习周报 化学 人教课标高二版(选修4) 2009-2010学年 第3期 总第159期 人教课标版(选修4) 题型:022
将煤转化为水煤气是通过化学方法将煤转化为洁净燃料的方法之一.煤转化为水煤气的主要反应为:
C+H2O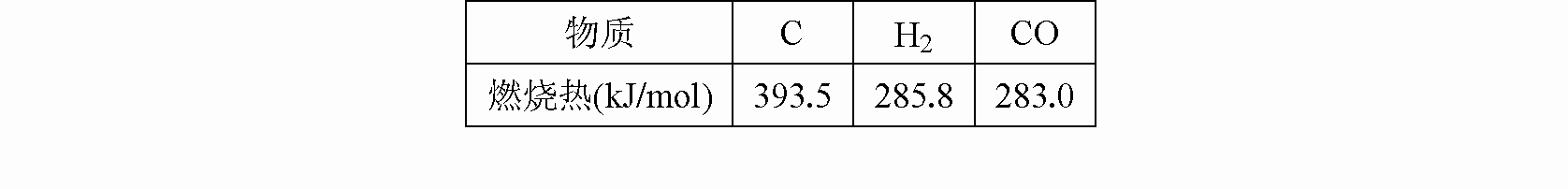
已知:
1 mol H2O(g)转化为1 mol H2O(l)放出44.0 kJ的热量.回答下列问题:(1)写出C不完全燃烧的热化学方程式:________.
(2)现有H2或CO为燃料提供热能,你认为应该选择________(填写序号);
a.H2 b.CO c.均可以理由是________.
(3)甲同学根据1 mol CO(g)和1 mol H2(g)完全燃烧放出的热量总和比1 mol C(s)完全燃烧放出的热量多,认为:“煤燃烧时加少量水,可以使煤燃烧放出更多的热量.”乙同学根据盖斯定律写出下列循环图:
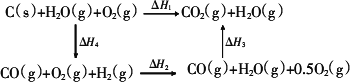
据此,乙同学认为:“将煤转化为水煤气再燃烧放出的热量与直接燃烧煤放出的热量一样多,而将煤转化为水煤气会增加生产环节、增加消耗,因此,将煤转化为水煤气得不偿失.”请你对甲、乙两同学的观点的正确性进行评价并阐述你的理由:
________.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com