
| A. | 卤素是典型的非金属元素,因此不能与其他非金属元素化合 | |
| B. | 卤素单质越活泼,其熔、沸点就越高 | |
| C. | 卤素单质都能和水剧烈反应 | |
| D. | 卤素单质都能和H2反应,且气态氢化物的稳定性随单质氧化性的增强而增强 |
分析 A.卤素单质具有氧化性,能与具有还原性的非金属单质反应;
B.卤族元素的非金属性越强对应的单质越活泼,卤族元素从上到下对应单质的熔沸点逐渐升高;
C.元素的非金属性越弱,越难以与水反应;
D.卤素单质都具有较强氧化性,可与氢气发生化合反应,元素的非金属性越强,气态氢化物越稳定.
解答 解:A.卤素单质具有氧化性,能与具有还原性的非金属单质反应,在一定条件下与H2、P等反应,故A错误;
B.卤族元素的非金属性越强对应的单质越活泼,卤族元素从上到下对应单质的熔沸点逐渐升高,活泼性减弱,故B错误;
C.元素的非金属性越弱,越难以与水反应,F2和冷水剧烈反应,但I2和水反应缓慢,故C错误;
D.卤素单质都具有较强氧化性,可与氢气发生化合反应,气态氢化物的稳定性随单质氧化性的增强而增强,故D正确.
故选D.
点评 本题考查卤素单质及其化合物的性质,题目难度不大,本题注意把握相关基础知识的积累.


科目:高中化学 来源: 题型:选择题
| A. | H2、D2互为同位素 | |
| B. | 氨分子中的化学键都为非极性共价键 | |
| C. | NH4Cl的电子式: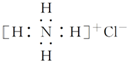 | |
| D. | S2-的结构示意图: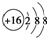 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 油脂在体内完全氧化时,提供的能量比糖类和蛋白质约高一倍 | |
| B. | 利用油脂在碱性条件下水解,可以生产甘油和肥皂 | |
| C. | 植物油通过氢化,即与氢气发生加成反应,可以制造植物奶油(人造奶油) | |
| D. | 天然油脂没有固定的熔沸点 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
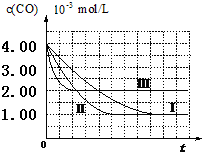 (I)目前,汽车厂商常利用催化技术将尾气中的NO和CO转化成CO2和N2,化学方程式如下:2NO+2CO$\stackrel{催化剂}{?}$2CO2+N2.为研究如何提高该转化过程反应速率,某课题组进行了以下实验探究.
(I)目前,汽车厂商常利用催化技术将尾气中的NO和CO转化成CO2和N2,化学方程式如下:2NO+2CO$\stackrel{催化剂}{?}$2CO2+N2.为研究如何提高该转化过程反应速率,某课题组进行了以下实验探究.| 实验编号 | 实验目的 | T/℃ | NO初始浓度 mol/L | CO初始浓度 mol/L | 同种催化剂的比表面积m2/g |
| Ⅰ | 为以下实验作参照 | 280 | 6.50×10-3 | 4.00×10-3 | 80 |
| Ⅱ | 探究催化剂比表面积对尾气转化速率的影响 | 6.50×10-3 | 4.00×10-3 | 120 | |
| Ⅲ | 探究温度对尾气转化速率的影响 | 360 | 6.50×10-3 | 4.00×10-3 | 80 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
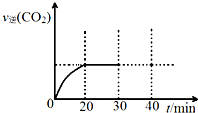 消除大气污染有多种方法.
消除大气污染有多种方法.| 浓度/mol•L-1 时间/min | NO | N2 | CO2 |
| 0 | 1.00 | 0 | 0 |
| 10 | 0.58 | 0.21 | 0.21 |
| 20 | 0.40 | 0.30 | 0.30 |
| 30 | 0.40 | 0.30 | 0.30 |
| 40 | 0.32 | 0.34 | 0.17 |
| 50 | 0.32 | 0.34 | 0.17 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 镁离子的电子式:Mg2+ | B. | HF的电子式:H:F | ||
| C. | Cl-离子的结构示意图: | D. | NH4Cl的电子式: |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4I的电子式: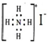 | |
| B. | Na2SiO3溶液与SO3的反应可用于推断Si与S的非金属性强弱 | |
| C. | 钠、锂分别在空气中燃烧,生成的氧化物中阴阳离子数目比不同 | |
| D. | Al2O3的化学键类型与AlCl3的化学键类型相同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com