
| A. | Mg | B. | N | C. | Be | D. | S |
分析 化合物WX能抑制水的电离说明是酸,则W为H,X为F或Cl元素,由于W、X、Y、Z是原子序数依次增大的四种短周期元素,说明X为F,化合物YZ2能促进水的电离说明是含弱离子的盐,水解促进水的电离,由化学式可知Y为金属阳离子,且+2价离子,则Y是Mg,Z是Cl元素.
解答 解:化合物WX能抑制水的电离说明是酸,则W为H,X为F或Cl元素,由于W、X、Y、Z是原子序数依次增大的四种短周期元素,说明X为F,化合物YZ2能促进水的电离说明是含弱离子的盐,水解促进水的电离,由化学式可知Y为金属阳离子,且+2价离子,原子序数大于氟,则Y是Mg,Z是Cl元素,故选A.
点评 本题考查位置性质关系,根据短周期元素形成的化合物WX能抑制水的电离,推断W、X是关键,注意理解水的电离平衡的影响因素,难度中等.


 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 强氧化性和脱水性 | B. | 强氧化性和吸水性 | ||
| C. | 难挥发性和酸性 | D. | 脱水性和吸水性 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
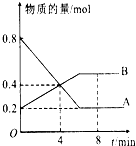 某温度时,在2L容器中A、B两种物质间的转化反应中A、B物质的量随时间变化的曲线如图所示,由图中数据
某温度时,在2L容器中A、B两种物质间的转化反应中A、B物质的量随时间变化的曲线如图所示,由图中数据查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 为测定某NaOH溶液的浓度,通常用已润洗的酸式滴定管放出25.00mL标准盐酸溶液于锥形瓶中,加2滴酚酞,然后向已润洗的碱式滴定管中注入未知浓度的NaOH溶液进行滴定 | |
| B. | 用无水CuSO4 、BaCl2溶液、稀盐酸、NaOH溶液、红色石蕊试纸、KSCN溶液、新制氯水等试剂可确定摩尔盐的化学式 | |
| C. | 通常采用产生气泡的快慢,来比较不同条件下Na2S2O3溶液与稀硫酸的反应速率 | |
| D. | 萃取操作所用的分液漏斗使用前应加入少量水,见旋塞芯处是否漏水,待确认不漏水后则可以使用 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 为除去FeSO4溶液中的Fe2(SO4)3,可加入铁粉,再过滤 | |
| B. | 为除去溴苯中的溴,可用NaOH溶液洗涤,再分液 | |
| C. | 为除去乙炔气中少量的H2S,可使其通过CuSO4 溶液 | |
| D. | 为除去CO2 中少量的SO2 ,可使其通过饱和Na2CO3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子式为C10H1202的有机物,①苯环上有两个取代基,②能与NaHCO3反应生成气体,满足以上2个条件的该有机物的同分异构体有15种 | |
| B. | 分子式为C4H8Cl2机物,只含有一个甲基的同分异构体有7种 | |
| C. | 分子式为C4H10O的醇,能在铜催化下被O2氧化为醛的同分异构体有4种 | |
| D. |  分子中的所有原子有可能共平面 分子中的所有原子有可能共平面 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 铜片消耗完所需时间 | |
| B. | 反应中氧化剂得到电子总数 | |
| C. | 反应后溶液中铜离子浓度(反应后溶液体积不变) | |
| D. | 反应生成气体的体积(同温、同压) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
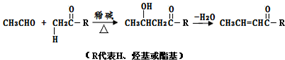
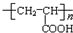 +HOCH2CH2OH$→_{△}^{浓硫酸}$
+HOCH2CH2OH$→_{△}^{浓硫酸}$ +2H2O.
+2H2O.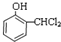 +NaOH→
+NaOH→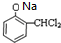 +H2O.
+H2O.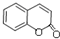 .
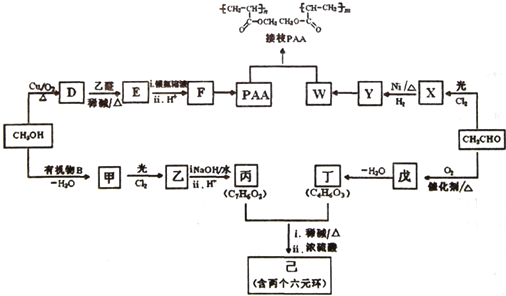
.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com