


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案 目标测试系列答案
目标测试系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在电解池的阳极发生氧化反应 |
| B、与电源负极相接的是电解池的阴极 |
| C、电子从电源的负极沿导线流向电解池的阴极 |
| D、与电源正极相接的是电解池的阴极 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、棉花、木材和植物秸秆的主要成分都是纤维素 |
| B、含钙、钡、铂等金属元素的物质有绚丽的颜色,可用于制造焰火 |
| C、PM 2.5亦称可入肺颗粒物,分散在空气中形成胶体,表面积大,能吸附有毒有害物质 |
| D、水结冰是从上向下,而油脂凝固是从下向上进行,这一现象合理的解释是因为油脂密度大于水的密度 |
查看答案和解析>>
科目:高中化学 来源: 题型:
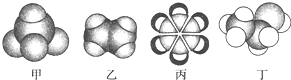
| A、甲能使酸性KMnO4溶液褪色 |
| B、乙可与溴水发生取代反应而使溴水褪色 |
| C、丙中的碳碳键是介于碳碳单键和碳碳双键之间的独特键 |
| D、丁在稀硫酸作用下可与乙酸发生取代反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na+、NO3-、Mg2+、Cl- |
| B、Na+、CO32-、NO3-、Ca2+ |
| C、K+、Cl-、SO42-、Cu2+ |
| D、Ba2+、Cl-、K+、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com