
(20分)
20-Ⅰ(6分)固硫剂是把煤燃烧时生成的二氧化硫以盐的形式固定在炉渣中的物质,可
减少二氧化硫对大气的污染。下列物质中可用做固硫剂的有
A.CaO B.Na2C03 C.NH4N03 D. P205
20-Ⅱ(14分)以黄铁矿为原料,采用接触法生产硫酸的流程可简示如下:
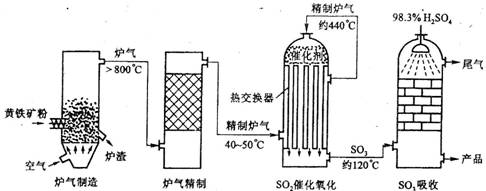
请回答下列问题:
(1)在炉气制造中,生成S02的化学方程式为______________________________;
(2)炉气精制的作用是将含S02的炉气_______________、_______________及干燥,如果炉气不经过精制,对S02催化氧化的影响是 _____________ _______________ :

(3)精制炉气(含SO2体积分数为7%、O2为ll%、N2为82%)中S02平衡转化率与温度及压强关系如下图所示。在实际生产中,S02催化氧化反应的条件选择常压、450℃;左右(对应图中A点),而没有选择S02转化率更高的B或C点对应的反应条件,其原因分别是______________________________、______________________________;
(4)在S02催化氧化设备中设置热交换器的目的是_______________、_______________,从而充分利用能源。
20-I A、B
20-II
(1)4FeS2 + 11O2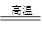 2Fe2O3 + 8SO2
2Fe2O3 + 8SO2
(2)除尘、水洗;矿尘,砷、硒等化合物使催化剂中毒,水蒸气对设备和生产有不良影响。
(3)不选B点,因为压强越大对设备的投资大,消耗的动能大;SO2原料的转化率在1个大气压下的转化率已是97%左右,再提高压强,SO2转化率提高的余地很小,所以采用常压。
不选C点,因为温度越低,SO2转化率虽然更高,但催化剂的催化作用受影响,450℃时,催化剂的催化效率最高。故选择A点,不选C点
(4)利用反应放出的热量预热原料气体;上层反应气经热交换器温度降到400~500℃进入下层使反应更加完全。
【解析】


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:阅读理解
 实验室中有一未知浓度的稀盐酸,某学生为测定盐酸的浓度在实验室中进行如下实验.请你完成下列填空:
实验室中有一未知浓度的稀盐酸,某学生为测定盐酸的浓度在实验室中进行如下实验.请你完成下列填空:| 实验编号 | NaOH溶液的浓度 (mol/L) |
滴定完成时,消耗NaOH溶液的体积(mL) | 待测盐酸溶液的体积(mL) |
| 1 | 0.10 | 20.02 | 20.00 |
| 2 | 0.10 | 20.00 | 20.00 |
| 3 | 0.10 | 19.00 | 20.00 |
| 4 | 0.10 | 19.98 | 20.00 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解

| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 1mol CH3OCH3、1mol H2O | 2mol CH3OH | 1mol CH3OH |
| CH3OH的浓度(mol/L) | c1 | c2 | c3 |
| 反应的能量变化 | 吸收a kJ | 放出b kJ | 放出c kJ |
| 平衡时体积(L) | V1 | V2 | V3 |
| 反应物转化率 | α 1 | α 2 | α 3 |

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
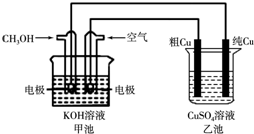 粗铜中一般含有锌、铁、银、金等杂质.在下图所示的装置中,甲池的总反应方程式为:2CH3OH+3O2+4KOH═2K2CO3+6H2O 接通电路一段时间后,纯Cu电极质量增加了3.2g.在此过程中,下列说法正确的是( )
粗铜中一般含有锌、铁、银、金等杂质.在下图所示的装置中,甲池的总反应方程式为:2CH3OH+3O2+4KOH═2K2CO3+6H2O 接通电路一段时间后,纯Cu电极质量增加了3.2g.在此过程中,下列说法正确的是( )查看答案和解析>>
科目:高中化学 来源:2010年重庆一中高三下期第三次月考 题型:填空题
(20分)早在2004年,国家食品监督局就发出“警惕食品中丙烯酰胺(CH2=CHCONH2)”的公告,丙烯酰胺会在长期炸制食物过程中产生,具有中等毒性,它对人体可造成神经毒性和遗传毒性。已知:有机物H是丙烯酰胺的相邻同系物;A为气态烃,标准状况下密度为2.5g / L,其分子中有2个甲基;F为六元环状化合物。回答下列问题:
(1)写出G的结构简式__________________ K的结构简式_____________________
(2)指明下列反应类型:A→B:___________________E→G:___________________
(3)写出下列化学方程式:
C→D______________________________________________________________
E→F_______________________________________________________________
(4)下列关于丙烯酰胺的说法,不正确的是________(填选项序号)
①丙烯酰胺所有碳、氮原子不可能在一个平面内 ②人们应改善膳食习惯,少食油炸食品
③丙烯酰胺可发生加成和水解反应 ④酰胺类物质其实就是蛋白质
(5)写出有机物H所有同种类别的同分异构体的结构简式:
__________________________________________________________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com