
【题目】现有 A、B、C、D、E、F 六种短周期主族元素,其相关性质信息如下:
元素 | 相关信息 |
A | 地壳中含量最多的金属元素 |
B | 原子核外电子数和周期序数相等 |
C | 最外层电子数是次外层电子数的 3 倍 |
D | 最高正价与最低负价代数和为 4,常温下单质为固体 |
E | 在短周期元素中,原子半径最大 |
F | M 层比L 层少 1 个电子 |
请根据上述信息,完成下列问题:
(1)请给出元素 D 在元素周期表中的位置:________。
(2)请将 A、D、E、F 四种元素的简单离子按照离子半径由大到小排序(用离子符号表示):__________。
(3)请给出化合物 BFC 的电子式:______。
(4)用电子式表示 E 与 F 形成化合物 EF 的过程:______。
(5)请将 A、D、F 三种元素的最高价氧化物对应的水化物按照酸性由强到弱排序(用化学式表示):__________。
(6)元素 A 的单质常用于野外焊接钢轨,请写出该反应的化学方程式:________。
(7)单质 A 能溶于 E 的最高价氧化物对应水化物的水溶液,请给出该反应的离子方程式:_____________。
【答案】第三周期 VIA 族 S2- > Cl- > Na+ > Al3+ ![]()
 HClO4 > H2SO4> Al(OH)3 2Al + Fe2O3
HClO4 > H2SO4> Al(OH)3 2Al + Fe2O3![]() Al2O3 + 2Fe 2Al + 2OH- + 2H2O=2
Al2O3 + 2Fe 2Al + 2OH- + 2H2O=2![]() + 3H2↑
+ 3H2↑
【解析】
A为地壳中含量最多的金属元素,则A为Al;B的原子核外电子数和周期序数相等,则B为H;C原子的最外层电子数是次外层电子数的 3 倍,则C为O;D的最高正价与最低负价代数和为 4,常温下单质为固体,则D为S;E在短周期元素中,原子半径最大,则E为Na;F原子的M 层比L 层少 1 个电子,则F为Cl。
(1)元素 D 为S,电子排布为2、8、6,在元素周期表中的位置:第三周期 VIA 族。答案为:第三周期 VIA 族;
(2)A、D、E、F 分别为Al、S、Na、Cl,四种元素的简单离子中,S2-、Cl-比Na+、Al3+多一个电子层,按照离子半径由大到小排序为:S2- > Cl- > Na+ > Al3+。答案为:S2- > Cl- > Na+ > Al3+;
(3)化合物 BFC 的化学式为HClO,电子式为![]() 。答案为:
。答案为:![]() ;
;
(4) E 与 F 分别为Na、Cl,形成化合物 NaCl的过程为 。答案为:
。答案为: ;
;
(5)A、D、F 三种元素分别为Al、S、Cl,非金属性越强,最高价氧化物对应的水化物的酸性越强,所以按照酸性由强到弱排序(用化学式表示)为:HClO4 > H2SO4> Al(OH)3。答案为:HClO4 > H2SO4> Al(OH)3;
(6)元素 A 为Al,它的单质与氧化铁反应常用于野外焊接钢轨,该反应的化学方程式:2Al + Fe2O3![]() Al2O3 + 2Fe。答案为:2Al + Fe2O3
Al2O3 + 2Fe。答案为:2Al + Fe2O3![]() Al2O3 + 2Fe;
Al2O3 + 2Fe;
(7)单质 Al 能溶于 NaOH的水溶液,生成NaAlO2和H2,该反应的离子方程式为:2Al + 2OH- + 2H2O=2![]() + 3H2↑。答案为:2Al + 2OH- + 2H2O=2
+ 3H2↑。答案为:2Al + 2OH- + 2H2O=2![]() + 3H2↑。
+ 3H2↑。


 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案科目:高中化学 来源: 题型:
【题目】Fe、HCN与K2CO3在一定条件下发生如下反应:Fe+6HCN+2K2CO3=K4Fe(CN)6+H2↑+2CO2↑+2H2O,回答下列问题:
(1)此化学方程式中涉及的第二周期元素的电负性由小到大的顺序为________。
(2)配合物K4Fe(CN)6的中心离子的价电子排布图为______,该中心离子的配位数是_______。
(3)1mol HCN分子中含有σ键的数目为_______,HCN分子中碳原子轨道杂化类型是_______,与CN-互为等电子体的阴离子是_______。
(4)K2CO3中阴离子的空间构型为_________,其中碳原子的价层电子对数为____________。
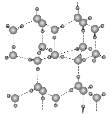
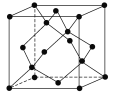
(5)冰的晶体结构模型如图,它的晶胞与金刚石相似,水分子之间以氢键相连接,在一个晶胞中有________个氢键,若氢键键长为d nm,则晶体密度(g·cm-3)计算式为_______ (用NA表示阿伏加德罗常数的值)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,浓度均为0.1 mol/L的溶液,其pH如下表所示。有关说法正确的是
序号 | ① | ② | ③ | ④ |
溶液 | NaCl | CH3COONH4 | NaF | NaHCO3 |
pH | 7.0 | 7.0 | 8.1 | 8.4 |
A.酸性强弱:H2CO3>HF
B.①和②中溶质均未水解
C.离子的总浓度:①>③
D.④中:c(HCO3-) + 2c(CO32-) + c(H2CO3)![]() 0.1 mol/L
0.1 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应2NO2N2O4(g) H<0。将一定量的NO2充入注射器中并密封,改变活塞位置的过程中,气体透光率随时间的变化如图所示(气体颜色越深,透光率越小)。下列说法不正确的是
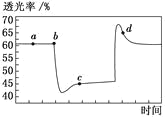
A.b 点的操作是压缩注射器
B.c 点与a点相比,c(NO2)增大、c(N2O4)减小
C.d 点:υ(正)<υ(逆)
D.若在c点将温度降低,其透光率将增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】科学发展是旧理论不断被质疑、被打破的过程。苯曾被认为是“环己三烯”的结构,后经修正成为我们今天所学的理论。如图列举了几种常见的环状多烯结构,下列说法正确的是( )
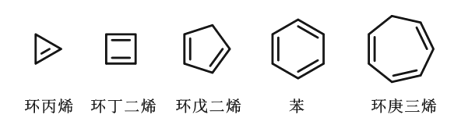
A.环丙烯、环丁二烯和环戊二烯均可分别实现所有碳原子共平面
B.上述五种化合物均可使溴的四氯化碳溶液褪色
C.上述五种化合物互为同系物,化学性质相似
D.依照上述环状多烯的结构规律,可以推测“环辛四烯”的分子式为C8H10
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)已知水在25℃和100℃时,其电离平衡曲线如图所示:
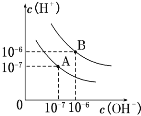
①则25℃时水的电离平衡曲线应为_____。(填“A”或“B”)
②25℃下,下列三种溶液中,由水电离出的氢离子的物质的量浓度之比a:b:c=_____。
a.pH=1的盐酸b.pH=2的盐酸c.pH=12的NaOH溶液
③25℃下,若VaLpH=a的盐酸与VbLpH=b的NaOH溶液恰好中和,a+b=13,则Va:Vb=_____。
(2)某温度(t℃)时,测得0.01mol·L-1的NaOH溶液的pH=13。
①该温度下水的Kw=_____。
②此温度下,将pH=1的盐酸溶液VaL与pH=14的NaOH溶液VbL混合(忽略体积变化),混合后溶液的pH为2,则Va:Vb=_____。
(3)下列说法中正确的是_____。
a.25℃时,pH=12的氨水和pH=2的H2SO4溶液等体积混合,所得溶液pH>7
b.100℃时,pH=12的NaOH溶液和pH=2的H2SO4溶液恰好中和,所得溶液pH=7
c.25℃时,由水电离出的氢离子浓度为1×10-10mol/L的溶液中可能大量存在NH4+和Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.CaCO3溶于CH3COOH溶液中,反应的离子方程式为:CaCO3+2H+=Ca2++CO2↑+H2O
B.向AlCl3溶液中通入过量NH3,反应的离子方程式为:Al3++4OH-=![]() +2H2O
+2H2O
C.下列四种离子因发生氧化还原反应而不能大量共存:K+、Fe3+、SCN-、Cl-
D.向稀硫酸中滴入Ba(OH)2溶液,反应的离子方程式为:Ba2++2OH-+2H++![]() =2H2O+BaSO4↓
=2H2O+BaSO4↓
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式正确的是 ( )
A. 向稀HNO3中滴加Na2SO3溶液:SO32-+2H+=SO2↑+H2O
B. 少量SO2通入氢氧化钠溶液中:OH-+SO2=HSO3-
C. 加热可增强纯碱溶液去污能力:CO32-+2H2O![]() H2CO3+2OH-
H2CO3+2OH-
D. 用惰性电极电解CuSO4溶液:
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外小组分别用如图所示装置对原电池和电解原理进行实验探究。

请回答:
Ⅰ.用图 1 所示装置进行第一组实验。
(1)在保证电极反应不变的情况下,不能替代 Cu 作电极的是__(填字母序号)。
A 铝 B 石墨 C 银 D 铂
(2)N 极发生反应的电极反应式为__。
Ⅱ.用图 2 所示装置进行第二组实验。实验过程中,观察到与第一组实验不同的现象:两极均有气体产生,Y极区溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍然澄清。 查阅资料得知,高铁酸根离子(FeO42-)在溶液中呈紫红色。
(3)电解过程中,X 极区溶液的 pH__(填“增大”“减小”或“不变”)。
(4)电解过程中,Y 极发生的电极反应之一为 Fe﹣6e﹣+8OH﹣= FeO42-+4H2O 若在 X 极收集到672 mL 气体,在 Y 极收集到 168 mL 气体(均已折算为标准状况时气体体积),则 Y 电极(铁电极)质量减少____g。
(5)在碱性锌电池中,用高铁酸钾作为正极材料,电池反应为 2K2FeO4+3Z=Fe2O3+ZnO+2K2ZnO2,该电池正极发生的反应的电极反应式为__。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com