
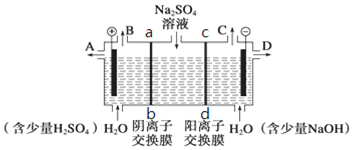
分析 ①阴极上氢离子放电,则NaOH在阴极生成;根据阴阳离子的移动方向,通过相同电量时,阴阳离子交换的个数判断;
②水电离生成的氢离子放电,而氢氧根离子不放电;
③阳极是氢氧根离子放电生成氧气,生成1mol氧气转移4mol的电子,由此分析解答.
解答 解:①阴极上氢离子放电,则NaOH在阴极生成,由图可知,D在阴极附近,制得的氢氧化钠溶液从D出口导出;
阳极氢氧根离子放电,因此硫酸根离子向阳极移动,阴极氢离子放电,因此钠离子向阴极移动,所以通过相同电量时,通过阴离子交换膜的离子数小于通过阳离子交换膜的离子数,
故答案为:D;<;
②水电离出的氢离子在阴极放电,而氢氧根离子不放电,促进水的电离,导致溶液中氢氧根离子浓度增大,溶液的pH增大,
故答案为:H+在阴极放电,水的电离平衡正向移动,溶液中OH-浓度增大,pH增大;
③阳极是氢氧根离子放电生成氧气,生成1mol氧气转移4mol的电子,所以当电路中通过1mol电子的电量时,阳极生成氧气的物质的量为0.25mol,故答案为:0.25.
点评 本题考查电解池原理,明确离子放电顺序是解本题关键,根据各个电极上发生的反应来分析解答,把握电解质溶液的酸碱性确定生成的离子或物质,为易错点.


 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源: 题型:选择题

| A. | ⑤③① | B. | ②③④ | C. | ③⑤④ | D. | ③②① |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2+2OH-═CO32-+H2O | B. | Al2O3+2OH-+═2 AlO2-+H2O | ||
| C. | Al3++4OH-═AlO2-+2H2O | D. | 2 Al+2OH-+6H2O═2 AlO2-++3 H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO32-+H+=HCO3- | B. | HCO3-+3CO32-+7H+═4CO2↑+4H2O | ||
| C. | 2HCO3-+5CO32-+12H+═7CO2↑+7H2O | D. | HCO3-+CO32-+3H+═2CO2↑+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原气体中肯定有SO2,可能有HCl | B. | 原气体中肯定没有H2S、HBr和CO2 | ||
| C. | 原气体中肯定有SO2和 HCl | D. | 原气体中肯定没有CO2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 海水淡化------蒸馏 | |
| B. | 将碘单质从沙子提取出来--------过滤 | |
| C. | 盐水中获得食盐--------萃取分液 | |
| D. | 稀释浓硫酸时将水慢慢加入浓硫酸中 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com