
有一硝酸盐晶体,化学式为M(NO3)x·3H2O,经测定其摩尔质量为242 g·mol-1.将1.21 g此晶体溶于水,配成100 mL溶液.将此溶液置于电解池中用惰性材料作电极进行电解.当有0.01 mol电子通过电极时,溶液中全部金属离子在电极上析出,经测定A极增重0.32 g.
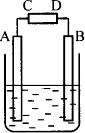
(1)C极为________极,B极产生的气体为________.
(2)M(NO3)x·H2O中x=________,M的相对原子质量为________.
(3)如果电解过程中溶液的体积不变,计算电解后溶液的c(H+)=________.
 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案 应用题作业本系列答案
应用题作业本系列答案科目:高中化学 来源: 题型:
(1)金属M的相对原子质量及x和n的值各是多少?
(2)若电解时溶液体积变化可忽略不计,则电解后溶液的pH是多少?
查看答案和解析>>
科目:高中化学 来源:2011-2012学年河南省南阳一中高二第一次月选4考化学试卷(带解析) 题型:计算题
(6分)有一硝酸盐晶体,分子式为M(NO3)x·nH2O,经测定其摩尔质量为
242g / mol。取1.21 g此晶体溶于水,配制成100 mL溶液。将其置于电解池中用惰性材料为电极进行电解。经测定,当有0.01 mol电子通过电极时,溶液中全部金属离子即在阴极上析出,电极增重0.32 g。计算:(写出计算过程)
(1) 1.21 g此盐晶体的物质的量是多少?x值是多少?
(2) 求M的相对原子质量和n值。
查看答案和解析>>
科目:高中化学 来源:2013届河南省高二第一次月选4考化学试卷(解析版) 题型:计算题
(6分)有一硝酸盐晶体,分子式为M(NO3)x·nH2O,经测定其摩尔质量为
242g / mol。取1.21 g此晶体溶于水,配制成100 mL溶液。 将其置于电解池中用惰性材料为电极进行电解。经测定,当有0.01 mol电子通过电极时,溶液中全部金属离子即在阴极上析出,电极增重0.32 g。计算:(写出计算过程)
(1) 1.21 g此盐晶体的物质的量是多少?x值是多少?
(2) 求M的相对原子质量和n值。
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)金属M的相对原子质量及x和n的值各是多少?
(2)若电解时溶液体积变化可忽略不计,则电解后溶液的pH是多少?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com