
| A. | 密度一定相同 | B. | 分子数一定相同 | ||
| C. | 原子数一定相同 | D. | 物质的量一定相同 |
分析 A.密度ρ=$\frac{M}{{V}_{m}}$,温度和压强影响气体摩尔体积;
B.CO和N2的摩尔质量相同,根据N=nNA=$\frac{m}{M}$NA分析;
C.二者都是双原子分子,结合N=nNA=$\frac{m}{M}$NA分析;
D.根据n=$\frac{m}{M}$分析二者的物质的量.
解答 解:A.密度ρ=$\frac{M}{{V}_{m}}$,由于气体摩尔体积不一定相同,则二者的密度不一定相同,故A错误;
B.CO和N2的摩尔质量为28g/mol,根据N=nNA=$\frac{m}{M}$NA可知,二者含有的分子数一定相同,故B正确;
C.CO和N2为双原子分子,根据B可知二者分子数相同,则含有原子数也一定相同,故C正确;
D.CO和N2的摩尔质量为28g/mol,根据n=$\frac{m}{M}$可知二者的物质的量一定相等,故D正确;
故选A.
点评 本题考查了物质的量的计算,题目难度不大,明确物质的量与摩尔质量、气体摩尔体积之间的关系为解答关键,注意掌握密度与摩尔质量之间的关系,试题培养了学生的灵活应用能力.


科目:高中化学 来源: 题型:多选题
| A. | 物质A的转化率小了 | B. | 平衡向正反应方向移动了 | ||
| C. | 物质B的质量分数减小了 | D. | b>a |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蒸发操作时,应使混合物中的水分完全蒸干后,再移走酒精灯停止加热 | |
| B. | 蒸馏实验中,温度计的水银球应插入液态混合物中 | |
| C. | 用酒精萃取溴水中的溴单质的操作可选用分液漏斗,而后静置分液 | |
| D. | 蒸馏时,蒸馏时冷凝水从冷凝管下口进上口出 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
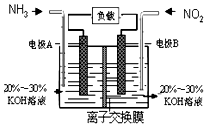 空气质量与我们的健康息息相关,目我国通过检测6项污染物的质量浓度来计算空气质量指数(AQI),SO2、NO2、和CO是其中3项中的污染物.
空气质量与我们的健康息息相关,目我国通过检测6项污染物的质量浓度来计算空气质量指数(AQI),SO2、NO2、和CO是其中3项中的污染物.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
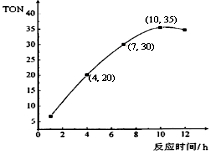 甲醇和CO2可直接合成DMC:2CH3OH(g)+CO2 (g)?CH3OCOOCH3 (g)+H2O(g),但甲醇转化率通常不会超过1%,制约该反应走向工业化生产.
甲醇和CO2可直接合成DMC:2CH3OH(g)+CO2 (g)?CH3OCOOCH3 (g)+H2O(g),但甲醇转化率通常不会超过1%,制约该反应走向工业化生产.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com