
���й������ʵ���Ũ�ȵı�������ȷ����
A��0.3 mol/L Na2SO4��Һ�к���Na+ ��SO42�������ʵ���Ϊ0.9mol
B����1Lˮ����22.4LNH3ʱ���ð�ˮ��Ũ�Ȳ���1 mol/L��ֻ�е�22.4L NH3����ˮ�Ƶ�1L��ˮʱ����Ũ�Ȳ���1 mol/L
C��10��ʱ0.5 mol/L��ϡ����100mL��������5gˮ����ȴ��10��ʱ�������С��100mL���������ʵ���Ũ�ȴ���0.5 mol/L
D��10��ʱ0.5 mol/L��KCl������Һ100mL��������5gˮ����ȴ��10��ʱ�������С��100 mL���������ʵ���Ũ����Ϊ0.5 mol/L

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2014�����ʡ�����и߶���ѧ�����л�ѧ���ģ��Ծ��������棩 ���ͣ�ѡ����
����������֬����;����
�������Ӫ������ ����ȡ���� ����ȡ���� ���Ʊ�����
A���٢ڢ� B���٢ۢ�
C���ڢۢܢ� D���٢ڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�����ʡ�人�и߶���ѧ������������ѧ�Ծ��������棩 ���ͣ������
��10�֣���������Ũ�Ⱦ�Ϊ0��05 mol/L��������Һ����Na2CO3 ��NaHCO3 ��HCl ��NH3��H2O���ش�������⣺��1��������Һ�У��ɷ���ˮ����� ������ţ�
��2��������Һ�У�������NaOH��Һ��Ӧ��������H2SO4��Һ��Ӧ����Һ�У�����Ũ�ȴ�С�Ĺ�ϵ
��3������м�������NH4Cl���壬��ʱc(NH4��/OH��)��ֵ ������������С�����䡱 ��
��4�������ۺܵ͢���Һ��Ϻ���Һǡ�ó����ԣ�����ǰ�۵���� �ܵ�����������ڡ��� ��С�ڡ����ڡ���
��5��ȡ10 mL�Ģ���Һ����ˮϡ�͵�500 mL�������Һ����ˮ�������c(H��)�� mol/L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�����ʡ�人�и߶���ѧ������������ѧ�Ծ��������棩 ���ͣ�ѡ����
һ������ϡ�����������п��Ӧ��Ϊ������Ӧ���ʣ��Ҳ�Ӱ����������������������ϡ�����м����������������ʣ�����һ�����ܴﵽĿ�ĵ���
A������ͭ���� B��ˮ C���������Һ D���Ȼ�����Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�����ʡ�人�и�һ��ѧ������������ѧ�Ծ��������棩 ���ͣ�ѡ����
��7�֣�������ͬ��ԭ������CO��CO2��������
��1��������֮��Ϊ______����̼ԭ����֮��Ϊ______����ԭ������Ϊ_______��
��2��ͬ��ͬѹʱ�������֮��Ϊ______���ܶ�֮��Ϊ______��
��3��ͬ��ͬ���ʱ����ѹǿ֮��Ϊ_____���ܶ�֮��Ϊ______��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�����ʡ�人�и�һ��ѧ������������ѧ�Ծ��������棩 ���ͣ�ѡ����
��xR2+ +yH+ +O2��mR3+ +nH2O�����ӷ���ʽ�У���m��R3+�ж���ȷ����
A��m��4��R3+����������
B��m��2y��R3+����������
C��m��2��R3+�ǻ�ԭ����
D��m��y��R3+�ǻ�ԭ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014���㽭ʡ���ݵ�����У�߶���ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�������
��6�֣���һ���¶��£���2molA��2molB���������Ϸ������Ϊ2L���ܱո��������У��������·�Ӧ��3A(g)+B(g)  xC(g)+2D(g) ��H<0��2minĩ��Ӧ�ﵽƽ�⣬����0.8molD�������C��Ũ��Ϊ0.4mol?L-1����ش�
xC(g)+2D(g) ��H<0��2minĩ��Ӧ�ﵽƽ�⣬����0.8molD�������C��Ũ��Ϊ0.4mol?L-1����ش�
��1��x��ֵΪ_______
��2��A��ת����Ϊ��(A)%=______ ________
��3�����¶��¸÷�Ӧ��ƽ�ⳣ��K=
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014���㽭ʡ���ݵ�����У�߶���ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
���������һ�����Ϳɳ���أ�����ͨ���ܵ����ȣ��õ���ܳ�ʱ�䱣���ȶ��ķŵ��ѹ��������ص��ܷ�ӦΪ��3Zn+2K2FeO4+8H2O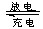 3Zn(OH)2+2Fe(OH)3+4KOH��������������ȷ���ǣ�
3Zn(OH)2+2Fe(OH)3+4KOH��������������ȷ���ǣ�
A���ŵ�ʱ������ӦΪ�� Zn-2e�D+2OH�D��Zn(OH)2
B�����ʱ������ӦΪ��Fe(OH)3-3e�D+5OH�D��FeO42-+4H2O
C���ŵ�ʱÿת��3mol���ӣ�������1molK2FeO4������
D���ŵ�ʱ�������ڳ��ʱ��ӵ�Դ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014��ӱ�ʡ������һ�С�������и߶���ѧ������������ѧ�Ծ��������棩 ���ͣ�ѡ����
���ڿ��淴Ӧ2AB3(g) A2(g)��3B2(g) ��H��0������ͼ����ȷ����
A2(g)��3B2(g) ��H��0������ͼ����ȷ����

�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com