
ЎѕМвДїЎїИзНјЛщКѕОЄДіТ»Т©ОпFµДєПіЙВ·ПЯЈє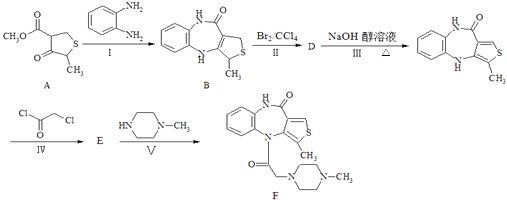
ЈЁ1Ј©AЦРє¬Сх№ЩДЬНЕµДГыіЖ·Ц±рКЗЎў Ј®
ЈЁ2Ј©ІЅЦиўт·ўЙъ·ґУ¦µДАаРНКЗ Ј®
ЈЁ3Ј©РґіцІЅЦиўуµД»ЇС§·ґУ¦·ЅіМКЅ Ј®
ЈЁ4Ј©РґіцН¬К±ВъЧгПВБРМхјюµДAµДТ»ЦЦН¬·ЦТм№№МеµДЅб№№јтКЅЈє Ј® ўЩІ»є¬јЧ»щЈ»
ўЪКЗ ![]() µДСЬЙъОпЈ¬ЗТ»·ЙПЦ»УРТ»ёцИЎґъ»щЈ»
µДСЬЙъОпЈ¬ЗТ»·ЙПЦ»УРТ»ёцИЎґъ»щЈ»
ўЫДЬ·ўЙъТшѕµ·ґУ¦єНЛ®Ѕв·ґУ¦ЈЁІ»їјВЗ ![]() µД±д»ЇЈ©Ј®
µД±д»ЇЈ©Ј®
ЈЁ5Ј©ЗлІОХХЙПГжєПіЙВ·ПЯЈ¬ТФјд¶юјЧ±ЅЎўClCH2COClЎўЈЁC2H5Ј©2NHОЄУР»ъФБПЈЁОЮ»ъКФјБИОСЎЈ©єПіЙ  Ј® МбКѕЈєўЩ
Ј® МбКѕЈєўЩ ![]()
![]()
![]()
ўЪєПіЙВ·ПЯБчіМНјКѕАэЈєC2H5OH ![]() H2C=CH2
H2C=CH2![]()
![]() Ј®
Ј®
Ўѕґр°ёЎї
ЈЁ1Ј©хҐ»щЈ»фК»щ
ЈЁ2Ј©јУіЙ·ґУ¦
ЈЁ3Ј©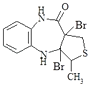 +2NaOH
+2NaOH 
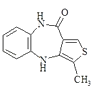 +2NaBr+2H2O
+2NaBr+2H2O
ЈЁ4Ј©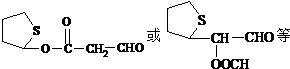
ЈЁ5Ј©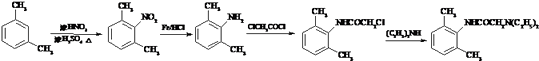
ЎѕЅвОцЎїЅвЈєёщѕЭМвЦРёчОпЦКЧЄ»Ї№ШПµЈ¬±ИЅПОпЦКBєН 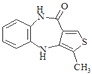 µДЅб№№ТФј°·ґУ¦ўтєНўуµДМхјюїЙЦЄЈ¬B·ўЙъјУіЙ·ґУ¦ЙъDЈ¬D·ўЙъПыИҐ·ґУ¦ЙъіЙ
µДЅб№№ТФј°·ґУ¦ўтєНўуµДМхјюїЙЦЄЈ¬B·ўЙъјУіЙ·ґУ¦ЙъDЈ¬D·ўЙъПыИҐ·ґУ¦ЙъіЙ  Ј¬ЛщТФDОЄ
Ј¬ЛщТФDОЄ 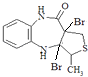 Ј¬±ИЅП
Ј¬±ИЅП 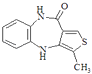 єНОпЦКFµДЅб№№ТФј°·ґУ¦ўфєНўхµДМхјюїЙЦЄЈ¬EОЄ
єНОпЦКFµДЅб№№ТФј°·ґУ¦ўфєНўхµДМхјюїЙЦЄЈ¬EОЄ 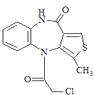 Ј¬ЈЁ1Ј©ёщѕЭAµДЅб№№јтКЅїЙЦЄЈ¬AЦРє¬Сх№ЩДЬНЕµДГыіЖ·Ц±рКЗхҐ»щЎўфК»щЈ¬ЛщТФґр°ёКЗЈєхҐ»щЈ»фК»щЈ»ЈЁ2Ј©ІЅЦиўт·ўЙъ·ґУ¦µДАаРНКЗјУіЙ·ґУ¦Ј¬ЛщТФґр°ёКЗЈєјУіЙ·ґУ¦Ј»ЈЁ3Ј©ІЅЦиўуµД»ЇС§·ґУ¦·ЅіМКЅОЄ
Ј¬ЈЁ1Ј©ёщѕЭAµДЅб№№јтКЅїЙЦЄЈ¬AЦРє¬Сх№ЩДЬНЕµДГыіЖ·Ц±рКЗхҐ»щЎўфК»щЈ¬ЛщТФґр°ёКЗЈєхҐ»щЈ»фК»щЈ»ЈЁ2Ј©ІЅЦиўт·ўЙъ·ґУ¦µДАаРНКЗјУіЙ·ґУ¦Ј¬ЛщТФґр°ёКЗЈєјУіЙ·ґУ¦Ј»ЈЁ3Ј©ІЅЦиўуµД»ЇС§·ґУ¦·ЅіМКЅОЄ 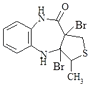 +2NaOH
+2NaOH 
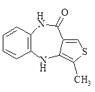 +2NaBr+2H2OЈ¬ЛщТФґр°ёКЗЈє
+2NaBr+2H2OЈ¬ЛщТФґр°ёКЗЈє  +2NaOH
+2NaOH 
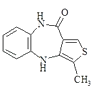 +2NaBr+2H2OЈ»ЈЁ4Ј©ВъЧгПВБРМхјюўЩІ»є¬јЧ»щЈ»ўЪКЗ
+2NaBr+2H2OЈ»ЈЁ4Ј©ВъЧгПВБРМхјюўЩІ»є¬јЧ»щЈ»ўЪКЗ ![]() µДСЬЙъОпЈ¬ЗТ»·ЙПЦ»УРТ»ёцИЎґъ»щЈ»ўЫДЬ·ўЙъТшѕµ·ґУ¦єНЛ®Ѕв·ґУ¦ЛµГчУРИ©»щєНхҐ»щЈ¬·ыєПМхјюµДAµДТ»ЦЦН¬·ЦТм№№МеµДЅб№№јтКЅОЄ
µДСЬЙъОпЈ¬ЗТ»·ЙПЦ»УРТ»ёцИЎґъ»щЈ»ўЫДЬ·ўЙъТшѕµ·ґУ¦єНЛ®Ѕв·ґУ¦ЛµГчУРИ©»щєНхҐ»щЈ¬·ыєПМхјюµДAµДТ»ЦЦН¬·ЦТм№№МеµДЅб№№јтКЅОЄ 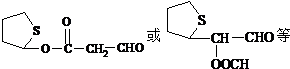 Ј¬ ЛщТФґр°ёКЗЈє
Ј¬ ЛщТФґр°ёКЗЈє  Ј»ЈЁ5Ј©ТФјд¶юјЧ±ЅЎўClCH2COClЎўЈЁC2H5Ј©2NHОЄУР»ъФБПєПіЙ
Ј»ЈЁ5Ј©ТФјд¶юјЧ±ЅЎўClCH2COClЎўЈЁC2H5Ј©2NHОЄУР»ъФБПєПіЙ 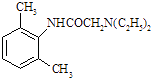 Ј¬їЙТФФЪјд¶юјЧ±ЅЙППИТэИлПх»щЈ¬ФЩ»№ФіЙ°±»щЈ¬АыУГClCH2COClЎўЈЁC2H5Ј©2NH·ўЙъМвЦРБчіМЦРµДІЅЦиўфєНўхјґїЙµГІъЖ·Ј¬єПіЙВ·ПЯОЄ
Ј¬їЙТФФЪјд¶юјЧ±ЅЙППИТэИлПх»щЈ¬ФЩ»№ФіЙ°±»щЈ¬АыУГClCH2COClЎўЈЁC2H5Ј©2NH·ўЙъМвЦРБчіМЦРµДІЅЦиўфєНўхјґїЙµГІъЖ·Ј¬єПіЙВ·ПЯОЄ 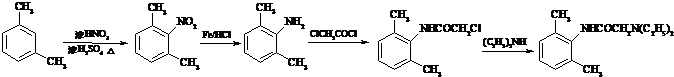 Ј¬
Ј¬
ЛщТФґр°ёКЗЈє 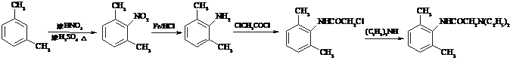 Ј®
Ј®



| Дкј¶ | ёЯЦРїОіМ | Дкј¶ | іхЦРїОіМ |
| ёЯТ» | ёЯТ»Гв·СїОіМНЖјцЈЎ | іхТ» | іхТ»Гв·СїОіМНЖјцЈЎ |
| ёЯ¶ю | ёЯ¶юГв·СїОіМНЖјцЈЎ | іх¶ю | іх¶юГв·СїОіМНЖјцЈЎ |
| ёЯИэ | ёЯИэГв·СїОіМНЖјцЈЎ | іхИэ | іхИэГв·СїОіМНЖјцЈЎ |
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїПВБРУР№ШКµСйµДСЎПоХэИ·µДКЗЈЁ Ј©
AЈ®ЕдЦЖ0.10molL©Ѓ1NaOHИЬТє | BЈ®іэИҐCOЦРµДCO2 | CЈ®±ЅЭНИЎµвЛ®ЦРI2 Ј¬ ·ЦіцЛ®ІгєуµДІЩЧч | DЈ®јЗВјµО¶ЁЦХµг¶БКэОЄ12.20mL |
|
|
|
|
A.A
B.B
C.C
D.D
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎї1996ДкїЖС§јТФЪУоЦжЦР·ўПЦБЛ H3·ЦЧУЈ¬H3єНH2КфУЪ
A.Н¬О»ЛШB.Н¬ЛШТмРОМеC.Н¬·ЦТм№№МеD.Н¬Т»ОпЦК
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїМмЅтёЫ±¬ХЁЦВґуБїЗи»ЇДЖЈЁNaCNЈ©Р№В¶Ј¬NaCNКЗѕз¶ѕОпЦКЈ®ЧЁјТГЗК№УГЛ«СхЛ®ЈЁH2O2Ј©Аґґ¦АнЗи»ЇДЖЈ¬·ґУ¦·ЅіМКЅИзПВЈєH2O2+NaCN+H2OЁTNaHCO3+NH3
ЈЁ1Ј©ИфУР0.49¶Ц NaCNР№В¶ЦБЙЩРиТЄЦКБї·ЦКэОЄ34%µДH2O2ИЬТє¶ЦЅшРРґ¦Ан ЈЁјЩЙиH2O2µДґ¦АнР§№ыКЗ100%Ј¬ЗТІ»їјВЗH2O2ЧФЙн·ЦЅвЈ©
ЈЁ2Ј©Па±ИУЪЛ«СхЛ®Ј¬ЖЇ°Ч·ЫЈЁЦчТЄіЙ·ЦCaЈЁClOЈ©2Ј©µДјЫёсТЄ±гТЛµД¶аЈ¬Ифґ¦АнПаН¬ЦКБїµДNaCNЈЁЙъіЙОпПаН¬Ј©РиТЄПыєДCaЈЁClOЈ©2molЈЁјЩЙиCaЈЁClOЈ©2µДґ¦АнР§№ыКЗ100%Ј©
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїТСЦЄAЎ«H ѕщОЄ¶МЦЬЖЪФЄЛШЎўЗл»ШґрПВБРОКМв:
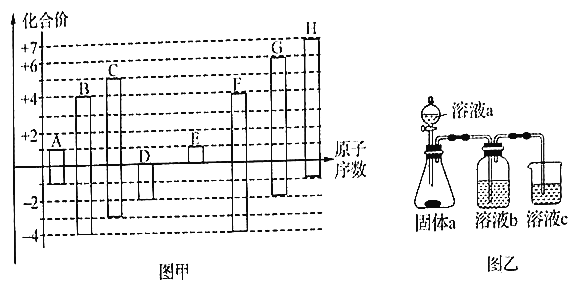
(1)FФЄЛШФЪЦЬЖЪ±нЦРµДО»ЦГОЄ________Ј¬A єНDРОіЙµДјИУРј«РФјьУЦУР·Зј«РФјьµД»ЇєПОпЈ¬ЖдµзЧУКЅОЄ________ ЎЈ
(2)DЎўEЎўGЎўH µДјтµҐАлЧУ°лѕ¶УЙґуµЅРЎµДЛіРтОЄ(Рґ»ЇС§КЅ) ________ ЎЈ
(3)УГµзЧУКЅ±нКѕіцEЎўH БЅЦЦФЄЛШЧйіЙµД»ЇєПОпµДРОіЙ№эіМ________ ЎЈ
(4)УГТТНјЧ°ЦГЦ¤ГчЛбРФ:HCl>H2CO3>H2SiO3Ј¬ФтИЬТєbОЄ________Ј»ИЬТєcЦРµДАлЧУ·ЅіМКЅОЄ________ЎЈПВБРКВКµїЙУГУЪ±ИЅПФЄЛШМјУлCl ·ЗЅрКфРФПа¶ФЗїИхµДКЗ________ЎЈ
a.ЧоёЯХэ»ЇєПјЫCl>C
b.C1µДЗв»ЇОп±ИC µДјтµҐЗв»ЇОпОИ¶Ё
C.C1µДЗв»ЇОп±ИC µДјтµҐЗв»ЇОп·РµгёЯ
d.ЧоёЯјЫСх»ЇОпµДЛ®»ЇОпµДЛбРФ:HC1O4>H2CO3
(5)AєНDРОіЙОЄ18µзЧУ·ЦЧУУлAєНGРОіЙµД13µзБЛ·ЦЧУ°ґ4 :1µДёцКэ±И·ґУ¦µДАлЧУ·ЅіМКЅОЄ________ЎЈ
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїУыФЪМъјЬМЁЙПУГХф·ўГујУИИХф·ўВИ»ЇДЖИЬТєЈ¬ПВБРІЩЧчЦРУ¦ЧоПИЅшРРµДКЗ
A.№М¶ЁМъИ¦B.µгИјѕЖѕ«µЖC.·ЕЦГѕЖѕ«µЖD.Ѕ«Хф·ўГу·ЕФЪМъИ¦ЙП
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїТСЦЄ¶ПБС1molC©ЃHјьЈ¬ТЄОьКХИИБї414.4kJЈ»¶ПБС1mol C©ЃCјьЈ¬ТЄОьКХИИБї347.4kJЈ»ЙъіЙ1mol CЁTCјьЈ¬»б·ЕіцИИБї615.3kJЈ»ЙъіЙ1mol H©ЃHјьЈ¬»б·ЕіцИИБї435.3kJЈ¬ДіУР»ъОп·ЦЅвµД·ґУ¦їЙ±нКѕОЄЈє 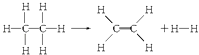
ИфФЪ·ґУ¦ЦРПыєДБЛ1molТТНйЈЁ·ґУ¦ОпЈ©Ј¬ФтУР№ШёГ·ґУ¦µДЛµ·ЁХэИ·µДКЗЈЁ Ј©
A.ёГ·ґУ¦·Еіц251.2 kJµДИИБї
B.ёГ·ґУ¦ОьКХ251.2 kJµДИИБї
C.ёГ·ґУ¦·Еіц125.6 kJµДИИБї
D.ёГ·ґУ¦ОьКХ125.6 kJµДИИБї
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїУР№ШНУлЕЁБтЛбµД·ґУ¦ПВБРЛµ·ЁґнОуµДКЗ
A. ёГ·ґУ¦ЦРСх»ЇјБУл»№ФјБОпЦКµДБїЦ®±ИОЄ1:1
B. ЕЁБтЛбФЪ·ґУ¦ЦРјИМеПЦіцСх»ЇРФЈ¬УЦМеПЦіцЛбРФ
C. ±кЧјЧґїцПВЈ¬lmolНєН2molЕЁБтЛбід·Ц·ґУ¦їЙµГ22.4LЖшМе
D. 1molНєНЧгБїЕЁБтЛб·ґУ¦Ј¬ЧЄТЖµзЧУёцКэОЄ2NA
Ійїґґр°ёєНЅвОц>>
їЖДїЈєёЯЦР»ЇС§ АґФґЈє МвРНЈє
ЎѕМвДїЎїЅ«Т»¶ЁБїµДРїУл100mL 18.5mol/L H2SO4ід·Ц·ґУ¦єуЈ¬РїНкИ«ИЬЅвЈ¬Н¬К±ЙъіЙЖшМеA 22.4LЈЁ±кЧјЧґїцЈ©Ј®Ѕ«·ґУ¦єуµДИЬТєПЎКНЦБ1LЈ¬ІвµГИЬТєµДpH=1Ј¬ФтПВБРРрКцЦРґнОуµДКЗЈЁ Ј©
A.ЖшМеAОЄSO2єНH2µД»мєПОп
B.·ґУ¦ЦР№ІПыєДZn 65g
C.ЖшМеAЦРSO2єНH2µДМе»э±ИОЄ1Јє4
D.·ґУ¦ЦР№ІЧЄТЖµзЧУ2mol
Ійїґґр°ёєНЅвОц>>
°Щ¶ИЦВРЕ - Б·П°ІбБР±н - КФМвБР±н
єю±±КЎ»ҐБЄНшОҐ·ЁєНІ»БјРЕПўѕЩ±ЁЖЅМЁ | НшЙПУРє¦РЕПўѕЩ±ЁЧЁЗш | µзРЕХ©ЖѕЩ±ЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРє¦РЕПўѕЩ±ЁЧЁЗш | ЙжЖуЗЦИЁѕЩ±ЁЧЁЗш
ОҐ·ЁєНІ»БјРЕПўѕЩ±Ёµз»°Јє027-86699610 ѕЩ±ЁУКПдЈє58377363@163.com