
| A.Na+ | B.Na | C.Cl | D.Cl- |
科目:高中化学 来源:不详 题型:单选题
| A.铍的原子失电子能力比镁弱 | B.砹(At)的氢化物不稳定 |
| C.硒化氢比硫化氢稳定 | D.Sr(OH)2比Ca(OH)2碱性强 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
①在含B的溶液中加入稀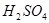 ,产生浅黄色浑浊和使澄清石灰水变浑浊的无色有刺激性气味的气体 ,产生浅黄色浑浊和使澄清石灰水变浑浊的无色有刺激性气味的气体 |
| ②20mL沸水中滴加F的饱和溶液1~2mL所得液体呈红褐色 |
| ③将实验②得到的红褐色液体加热蒸发,灼烧,最终得到红棕色固体 |
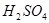 反应的离子方程式
反应的离子方程式 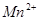 、
、 、
、 、
、 、
、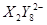 (C中含有的阴离子),
(C中含有的阴离子),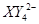 完成一个离子方程式,已知
完成一个离子方程式,已知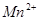 为还原剂,得到1mol
为还原剂,得到1mol 需氧化剂的物质的量为 mol
需氧化剂的物质的量为 mol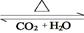 E,若有D和E ·
E,若有D和E ·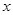 H2O的混合物13.04g,加热到完全反应后,气体产物通过浓H2SO4增重3.42g,剩余气体通过碱石灰增重2.20g,则混合物中D的质量为 g,E ·
H2O的混合物13.04g,加热到完全反应后,气体产物通过浓H2SO4增重3.42g,剩余气体通过碱石灰增重2.20g,则混合物中D的质量为 g,E ·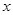
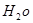 的化学式为
的化学式为 查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.(A-N+17m) mol | B.(A-N+17m) mol |
| C.(A-N) mol | D.(A-N) mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.该微粒不显电性 | B.该微粒质量数为4 |
| C.在周期表中与氢元素占同一位置 | D.该粒子质量比氢原子大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com