

 Al(OH)3+3H+µÄĘ½ŗā³£ŹżĪŖ £Ø±£ĮōĮ½Ī»ÓŠŠ§Źż×Ö£©£»
Al(OH)3+3H+µÄĘ½ŗā³£ŹżĪŖ £Ø±£ĮōĮ½Ī»ÓŠŠ§Źż×Ö£©£» H++OH££¬ŌņKw=1.0”Į10£14£»ÓÉÓŚAl(OH)3(s)
H++OH££¬ŌņKw=1.0”Į10£14£»ÓÉÓŚAl(OH)3(s)  Al3++3OH££¬ŌņKsp[Al(OH)3]=c(Al3+)?c3(OH£)=1.3”Į10£33£»ÓÉÓŚAl3++3H2O
Al3++3OH££¬ŌņKsp[Al(OH)3]=c(Al3+)?c3(OH£)=1.3”Į10£33£»ÓÉÓŚAl3++3H2O Al(OH)3+3H+£¬ŌņK=
Al(OH)3+3H+£¬ŌņK=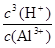 =
=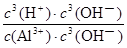 =
=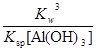 =
=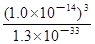 ”Ö7.7”Į10£10£»
”Ö7.7”Į10£10£»


| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā

 2I£+S4O62££©
2I£+S4O62££©
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
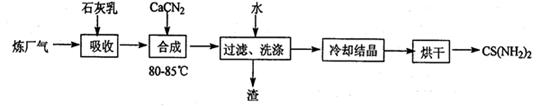
 2H2(g)+S2(g),ĘäĘ½ŗā³£Źż±ķ“ļŹ½ĪŖK=”£
2H2(g)+S2(g),ĘäĘ½ŗā³£Źż±ķ“ļŹ½ĪŖK=”£²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
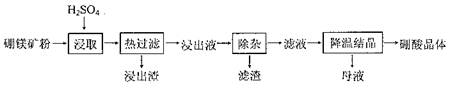
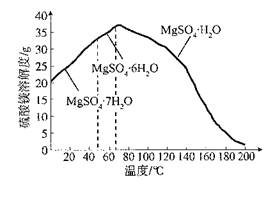
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®³ä·ÖĄūÓĆĢ«ŃōÄÜ |
| B£®ŅņµŲÖĘŅĖæŖ·¢ĄūÓĆ·ēÄÜ”¢Ė®ÄÜ”¢µŲČČÄÜ”¢³±Ļ«ÄÜ |
| C£®ŗĻĄķ”¢°²Č«æŖ·¢ĄūÓĆĒāÄÜ”¢ŗĖÄÜ |
| D£®ÄÜŌ“¶¼ŹĒĶعż»Æѧ·“Ó¦»ńµĆµÄ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
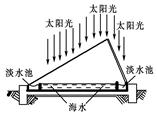
| A£®ĄūÓĆĢ«ŃōÄÜ£¬½«ŗ£Ė®ÕōĮóµ»Æ |
| B£®¼ÓČėĆ÷·Æ£¬Ź¹ŗ£Ė®µÄŃĪ·Ż³Įµķ²¢µ»Æ |
| C£®ĶØÖ±Į÷µē£¬²ÉÓƵēÉųĶø·ØŹ¹ŗ£Ė®µ»Æ |
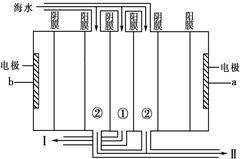
| D£®ĶعżĄė×Ó½»»»Ä¤£¬³żČ„Ėłŗ¬µÄŃĪ·ÖŹ¹ŗ£Ė®µ»Æ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®Ė®ĆŗĘų | B£®Ņ»Ńõ»ÆĢ¼ | C£®ĢģČ»Ęų | D£®ĒāĘų |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
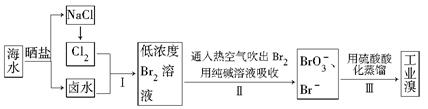

²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com