
 灵星计算小达人系列答案
灵星计算小达人系列答案 孟建平错题本系列答案
孟建平错题本系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
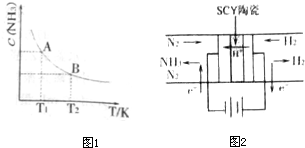
 科学家一直致力于“人工固氮”的新方法研究.
科学家一直致力于“人工固氮”的新方法研究.| 4 |
| 27 |
| 4 |
| 27 |
| c(NH3?H2O) |
| c(OH-) |
| c(NH4+)?c(OH-) |
| c(NH3?H2O) |
| c(H+) |
| c(OH-) |
| 时间/物质的量 | n(NH3) (mol) | n(O2 ) (mol) | n(NO) (mol) |
| 起始 | 1.600 | 3.200 | 0.000 |
| 第2min | a | 2.700 | 0.4000 |
| 第4min | 0.600 | 1.950 | 1.000 |
| 第6min | 0.600 | 1.950 | 1.000 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 3 |
| 2 |
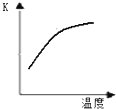
| T/K | 303 | 313 | 323 |
| NH3生成量/(10-6mol) | 4.8 | 5.9 | 6.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
在光照条件下,将体积相同的甲烷气体和Cl2(常温、常压下)混和,得到物质的量最多的是:
A.CH3Cl B.CH2Cl2 C.CHCl3
D.CCl4 E.HCl
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com