
对三联苯是一种有机合成中间体,工业上合成对三联苯的化学方程式为
3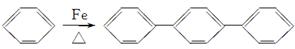 +2H2↑。下列说法不正确的是( )
+2H2↑。下列说法不正确的是( )
A.上述反应属于取代反应
B.对三联苯分子中至少有16个原子共平面
C.对三联苯的一氯取代物有4种
D.0.2 mol对三联苯在足量的氧气中完全燃烧消耗5.1 mol O2
科目:高中化学 来源: 题型:
已知C4H9Cl的核磁共振氢谱表明其只有一种化学环境的氢,则A的化学名称为__________________________________________________________。
(2)[2013·海南,18-Ⅱ(1)]已知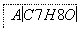
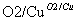
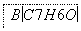 ,A的化学名称为________________________________________________________________________。
,A的化学名称为________________________________________________________________________。
(3)[2013·重庆理综,10(1)节选]CH3C≡CH的名称为
________________________________________________________________________。
(4)[2012·海南,18-Ⅱ(1)]化合物A是合成天然橡胶的单体,分子式为C5H8。A的结构简式为__________,化学名称是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关Fe2(SO4)3溶液的叙述正确的是( )
A.该溶液中,K+、Fe2+、C6H5OH、Br-可以大量共存
B.和KI溶液反应的离子方程式:Fe3++2I-===Fe2++I2
C.和Ba(OH)2溶液反应的离子方程式:Fe3++SO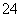 +Ba2++3OH-===Fe(OH)3↓+BaSO4↓
+Ba2++3OH-===Fe(OH)3↓+BaSO4↓
D.1 L 0.1 mol·L-1该溶液和足量的Zn充分反应,生成11.2 g Fe
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)丙烯的结构简式:C3H6( )
(2013·江苏,2A)
(2)将某气体通入溴水中,溴水颜色褪去,该气体一定是乙烯( )
(2013·江苏,13C)
(3)用酸性高锰酸钾溶液鉴别苯、环己烯和环己烷( )
(2013·海南,7D)
(4)环戊烷( )在光照下与氯气反应,只生成一种一氯代物( )
)在光照下与氯气反应,只生成一种一氯代物( )
(2013·海南,9B改编)
(5)乙烯、聚氯乙烯和苯分子中均含有碳碳双键( )
(2013·福建理综,7C)
(6)戊烷(C5H12)有两种同分异构体( )
(2013·福建理综,7B)
查看答案和解析>>
科目:高中化学 来源: 题型:
有A、B、C、D 4种烃,各取0.01 mol充分燃烧后,B、C、D所产生的二氧化碳均为448 mL(标准状况);A燃烧所得的二氧化碳是其他三者的3倍。在镍催化剂的作用下,A、B、C都能和氢气发生加成反应,B可以转变为C或D,C可以转变为D;B或C都能使酸性高锰酸钾溶液褪色,而A、D无此性质;在FeBr3存在时,A与溴发生取代反应。
试推断出4种烃的结构简式:
(1)A是________________,B是__________________,C是________________,D是________________。
(2)B→D的反应方程式:_____________________________________________。
(3)除去D中C的反应方程式:______________________________________。
(4)C发生加聚反应的方程式:________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
甲、乙两同学研究Na2SO3溶液与FeCl3溶液反应的情况。
| 步骤 | 操作 | 现象 |
| Ⅰ | 向2 mL 1 mol·L-1FeCl3溶液中加入一定量的Na2SO3溶液 | 溶液由棕黄色变为红褐色,并有少量刺激性气味的气体逸出 |
(1)常温下,FeCl3溶液的pH________7(填“<”、“>”或“=”)。
(2)分析红褐色产生的原因。
①甲同学认为步骤Ⅰ中溶液呈红褐色是因为生成了Fe(OH)3,用化学平衡移动原理解释溶液呈红褐色的原因:________________________________________________________________________。
②乙同学认为可能是发生了氧化还原反应,完成并配平其反应的离子方程式:
 Fe3++
Fe3++ SO
SO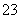 +
+ ________——
________—— Fe2++
Fe2++ ________+
________+ ________
________
 乙同学查阅资料得知:
乙同学查阅资料得知:
ⅰ.Fe2+与 反应生成墨绿色的絮状沉淀FeSO3;
反应生成墨绿色的絮状沉淀FeSO3;
ⅱ.墨绿色的FeSO3与黄色的FeCl3溶液混合后,溶液呈红褐色。
(3)甲同学为了确认溶液呈红褐色的原因是生成了Fe(OH)3,设计并完成了如下实验:
| 步骤 | 操作 | 现象 |
| Ⅱ | 用激光笔照射步骤Ⅰ中的红褐色溶液 | 出现“丁达尔效应” |
甲同学因此得出结论:溶液呈红褐色是因为生成了Fe(OH)3。而乙同学认为甲同学得出结论的证据仍然不足,乙同学的理由是________________________________________________________________________。
(4)为进一步确认Na2SO3溶液与FeCl3溶液反应的情况,乙同学设计并完成了如下实验:
| 步骤 | 操作 | 现象 |
| Ⅲ | 向1 mol·L-1的FeCl3溶液中通入一定量的SO2 | 溶液由黄色变为红褐色 |
| Ⅳ | 用激光笔照射步骤Ⅲ中的红褐色溶液 | 没有出现“丁达尔效应” |
①经检验步骤Ⅲ中红褐色溶液含有Fe2+,检验Fe2+选用的试剂是________(填字母)。
a.K3[Fe(CN)6]溶液
b.KSCN溶液
c.KMnO4溶液
②已知H2SO3是弱酸,请结合电离方程式说明步骤Ⅲ中出现红褐色的原因:________________________________________________________________________。
(5)结论:由上述实验得知,甲、乙两同学所持观点均正确。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com