
【题目】在含有弱电解质的溶液中,往往有多个化学平衡共存。
(1)一定温度下,向 1L 0.1mol·L-1 CH3COOH 溶液中加入 0.1molCH3COONa 固体,则溶液中![]() _____(填“增大”、“不变”或“减小”);写出该溶液中的电荷守恒关系_____。
_____(填“增大”、“不变”或“减小”);写出该溶液中的电荷守恒关系_____。
(2)土壤的 pH 一般在 4~9 之间。土壤中 Na2CO3 含量较高时,pH 可达 10.5,试用离子方程式解释土壤呈碱性的原因:_____。加入石膏(CaSO4·2H2O)可以使土壤碱性降低,有关反应的化学方程式为_____。
(3)水垢的主要成分 CaCO3 可以用过量食醋溶解,请结合化学用语,从沉淀溶解平衡的角度进行解释______________。
(4)常温下在 20mL0.1mol·L-1Na2CO3 溶液中逐滴加入 0.1mol·L-1HCl 溶液 40mL,溶液中含碳元素的各种微粒(CO2 因逸出未画出)物质的量分数(纵轴)随溶液 pH 变化的部分情况如图所示。回答下列问题:

①在同一溶液中 H2CO3 和CO![]() ____________________(填“能”或“不能”)大量共存。
____________________(填“能”或“不能”)大量共存。
②当 pH=7 时,溶液中含碳元素的最主要微粒为_____,溶液中各种离子的物质的量浓度的大小关系为_________。
③已知在 25℃时,CO![]() 水解反应的平衡常数
水解反应的平衡常数 =2.0×10-4,当溶液中c(HCO
=2.0×10-4,当溶液中c(HCO![]() ):c(CO
):c(CO![]() )=2:1 时,溶液的 pH=_____。
)=2:1 时,溶液的 pH=_____。
【答案】不变 c(CH3COO-)+c(OH-)=c(H+)+c(Na+) CO32-+H2O![]() HCO3-+OH-、HCO3-+H2O
HCO3-+OH-、HCO3-+H2O![]() H2CO3+OH- CaSO42H2O+Na2CO3=CaCO3+Na2SO4+2H2O CaCO3在溶液中存在溶解平衡CaCO3(s)
H2CO3+OH- CaSO42H2O+Na2CO3=CaCO3+Na2SO4+2H2O CaCO3在溶液中存在溶解平衡CaCO3(s)![]() Ca2+(aq)+CO32-(aq),加入过量食醋,食醋的主要成份醋酸电离出的氢离子与CO32-离子反应,CO32-浓度降低,水解平衡向右移动,使CaCO3溶解 不能 HCO3-、H2CO3 c(Na+)>c(Cl-)>c(HCO3-)> c(OH-)=c(H+) 10
Ca2+(aq)+CO32-(aq),加入过量食醋,食醋的主要成份醋酸电离出的氢离子与CO32-离子反应,CO32-浓度降低,水解平衡向右移动,使CaCO3溶解 不能 HCO3-、H2CO3 c(Na+)>c(Cl-)>c(HCO3-)> c(OH-)=c(H+) 10
【解析】
(1)CH3COOH的电离平衡常数K=![]() ,温度不变,电离平衡常数不变;混合溶液中存在电荷守恒关系c(CH3COO-)+c(OH-)=c(H+)+c(Na+);
,温度不变,电离平衡常数不变;混合溶液中存在电荷守恒关系c(CH3COO-)+c(OH-)=c(H+)+c(Na+);
(2)Na2CO3为强碱弱酸盐,CO32-在溶液中分步水解使土壤呈碱性,加入石膏后,CaSO4与Na2CO3反应生成CaCO3沉淀,CO32-浓度降低,水解平衡向左移动,OH-浓度降低,使土壤碱性降低;
(3)水垢的主要成分CaCO3在溶液中存在溶解平衡CaCO3(s)![]() Ca2+(aq)+CO32-(aq),加入过量食醋,食醋的主要成份醋酸电离出的氢离子与CO32-离子反应,CO32-浓度降低,水解平衡向右移动,使CaCO3溶解;
Ca2+(aq)+CO32-(aq),加入过量食醋,食醋的主要成份醋酸电离出的氢离子与CO32-离子反应,CO32-浓度降低,水解平衡向右移动,使CaCO3溶解;
(4)①由图象可以看出,H2CO3存在于PH<8的溶液中,CO32-存在于pH>8的溶液中;
②由图可知,H=7时溶液中c(OH-)=c(H+),溶液中含碳元素的主要微粒为HCO3-和H2CO3,此时溶液中溶质为NaCl、NaHCO3和H2CO3,由电荷守恒可知溶液中c(Na+)>c(Cl-),由碳酸钠与盐酸的反应可知溶液中c(Cl-)>c(HCO3-);
③CO32-的水解常数Kh=![]() =2.0×10-4可知,当溶液中c(HCO3-):c(CO32-)=2:1时,溶液中c(OH-)=1.0×10-4mol/L。
=2.0×10-4可知,当溶液中c(HCO3-):c(CO32-)=2:1时,溶液中c(OH-)=1.0×10-4mol/L。
(1)CH3COOH的电离平衡常数K=![]() ,温度不变,电离平衡常数不变;混合溶液中存在电荷守恒关系c(CH3COO-)+c(OH-)=c(H+)+c(Na+),故答案为:不变;c(CH3COO-)+c(OH-)=c(H+)+c(Na+);
,温度不变,电离平衡常数不变;混合溶液中存在电荷守恒关系c(CH3COO-)+c(OH-)=c(H+)+c(Na+),故答案为:不变;c(CH3COO-)+c(OH-)=c(H+)+c(Na+);
(2)Na2CO3为强碱弱酸盐,CO32-在溶液中分步水解使土壤呈碱性,水解的离子方程式为CO32-+H2O![]() HCO3-+OH-、HCO3-+H2O
HCO3-+OH-、HCO3-+H2O![]() H2CO3+OH-,加入石膏后,CaSO4与Na2CO3反应生成CaCO3沉淀,CO32-浓度降低,水解平衡向左移动,OH-浓度降低,使土壤碱性降低,使土壤碱性降低,反应方程式为CaSO42H2O+Na2CO3=CaCO3↓+Na2SO4+2H2O,故答案为:CO32-+H2O
H2CO3+OH-,加入石膏后,CaSO4与Na2CO3反应生成CaCO3沉淀,CO32-浓度降低,水解平衡向左移动,OH-浓度降低,使土壤碱性降低,使土壤碱性降低,反应方程式为CaSO42H2O+Na2CO3=CaCO3↓+Na2SO4+2H2O,故答案为:CO32-+H2O![]() HCO3-+OH-、HCO3-+H2O
HCO3-+OH-、HCO3-+H2O![]() H2CO3+OH-;CaSO42H2O+Na2CO3=CaCO3+Na2SO4+2H2O;
H2CO3+OH-;CaSO42H2O+Na2CO3=CaCO3+Na2SO4+2H2O;
(3)醋酸的酸性强于碳酸,水垢的主要成分CaCO3在溶液中存在溶解平衡CaCO3(s)![]() Ca2+(aq)+CO32-(aq),加入过量食醋,食醋的主要成份醋酸电离出的氢离子与CO32-离子反应,CO32-浓度降低,水解平衡向右移动,使CaCO3溶解,故答案为:CaCO3在溶液中存在溶解平衡CaCO3(s)
Ca2+(aq)+CO32-(aq),加入过量食醋,食醋的主要成份醋酸电离出的氢离子与CO32-离子反应,CO32-浓度降低,水解平衡向右移动,使CaCO3溶解,故答案为:CaCO3在溶液中存在溶解平衡CaCO3(s)![]() Ca2+(aq)+CO32-(aq),加入过量食醋,食醋的主要成份醋酸电离出的氢离子与CO32-离子反应,CO32-浓度降低,水解平衡向右移动,使CaCO3溶解;
Ca2+(aq)+CO32-(aq),加入过量食醋,食醋的主要成份醋酸电离出的氢离子与CO32-离子反应,CO32-浓度降低,水解平衡向右移动,使CaCO3溶解;
(4)①由图象可以看出,H2CO3存在于PH<8的溶液中,CO32-存在于pH>8的溶液中,二者不能大量共存于同一溶液中,故答案为:不能;
②由图可知,pH=7时溶液中c(OH-)=c(H+),溶液中含碳元素的主要微粒为HCO3-和H2CO3,此时溶液中溶质为NaCl、NaHCO3和H2CO3,由电荷守恒c(Na+)+c(H+)=c(Cl-)+c(HCO3-)+c(OH-)可知,溶液中c(Na+)>c(Cl-),由反应Na2CO3+HCl=NaCl+NaHCO3和NaHCO3+HCl=NaCl+ H2CO3可知,溶液中c(Cl-)>c(HCO3-),则溶液中各种离子的物质的量浓度的大小关系为c(Na+)>c(Cl-)>c(HCO3-)> c(OH-)=c(H+),故答案为:HCO3-、H2CO3;c(Na+)>c(Cl-)>c(HCO3-)> c(OH-)=c(H+);
③CO32-的水解常数Kh=![]() =2.0×10-4可知,当溶液中c(HCO3-):c(CO32-)=2:1时,溶液中c(OH-)=1.0×10-4mol/L,则溶液中c(H+)=
=2.0×10-4可知,当溶液中c(HCO3-):c(CO32-)=2:1时,溶液中c(OH-)=1.0×10-4mol/L,则溶液中c(H+)=![]() =10-10mol/L,溶液pH=10,故答案为:10。
=10-10mol/L,溶液pH=10,故答案为:10。


科目:高中化学 来源: 题型:
【题目】![]() 时,向
时,向![]() 恒容密闭容器中充入
恒容密闭容器中充入![]() 乙苯,发生反应:
乙苯,发生反应:
![]()
![]() 。
。
经一段时间后达到平衡,反应过程中测定的部分数据见下表:
时间 | 0 | 10 | 20 | 30 | 40 |
|
|
|
|
|
|
|
|
|
|
|
|
下列说法正确的是![]()
![]()
A.前![]() ,
,![]()
B.若保持其他条件不变,升高温度,平衡时![]() 乙苯
乙苯![]() ,则
,则![]()
C.保持其他条件不变,向容器中充入不参与反应的水蒸气作为稀释剂,则乙苯的转化率为![]()
D.相同温度下,起始时向容器中充入![]() 乙苯、
乙苯、![]() 苯乙烯和
苯乙烯和![]() ,达到平衡前
,达到平衡前![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在不同条件下,![]() 的密闭容器中发生如下反应
的密闭容器中发生如下反应![]() 。已知Y、Z的起始浓度为0,X的浓度
。已知Y、Z的起始浓度为0,X的浓度![]() 随反应时间
随反应时间![]() 变化的情况如下表:
变化的情况如下表:

下列说法不正确的是![]()
![]()
A.![]()
B.与实验1比较,实验2反应速率加快,原因可能是加入了合适的催化剂或增大体系压强
C.在实验3中,![]() 时间段内反应体系总共减少的X的物质的量为
时间段内反应体系总共减少的X的物质的量为![]()
D.若![]() ,则可说明
,则可说明![]() 的
的![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO和H2在一定条件下合成甲醇的反应为;CO(g)+2H2(g)![]() CH3OH(g) △H1。现在容积均为1L的a、b、c、d、e五个密闭容器中分别充入1molCO和2molH2的混合气体,控制温度,进行实验,测得相关数据如图(图1:温度分别为300℃ 、500℃的密闭容器中,甲醇的物质的量:图2:温度分别为Tl~T5的密闭容器中,反应均进行到5min时甲醇的体积分数)。下列叙述正确的是
CH3OH(g) △H1。现在容积均为1L的a、b、c、d、e五个密闭容器中分别充入1molCO和2molH2的混合气体,控制温度,进行实验,测得相关数据如图(图1:温度分别为300℃ 、500℃的密闭容器中,甲醇的物质的量:图2:温度分别为Tl~T5的密闭容器中,反应均进行到5min时甲醇的体积分数)。下列叙述正确的是

A. 该反应的△H1>0,且K1>K2
B. 将容器c中的平衡状态转变到容器d中的平衡状态,可采取的措施有升温或加压
C. 300℃时,向平衡后的容器中再充入0.8molCO, 0.6molH2,0.2molCH3OH,平衡正向移动
D. 500℃时,向平衡后的容器中再充入1molCH3OH,重新平衡后,H2浓度和百分含量均增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将0.1 mol/L CH3COOH溶液加水稀释或加入少量CH3COONa晶体时,都会引起( )
A. 溶液的pH增大
B. CH3COOH电离度增大
C. 溶液的导电能力减弱
D. 溶液中c(OH-)减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列我国科技成果所涉及物质的应用中,发生的不是化学变化的是
|
|
|
|
A.甲醇低温所制氢气用于新能源汽车 | B.氘、氚用作“人造太阳”核聚变燃料 | C.偏二甲肼用作发射“天宫二号”的火箭燃料 | D.开采可燃冰,将其作为能源使用 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以硫铁矿(主要成分为FeS2)为原料制备氯化铁晶体(FeCl3·6H2O)的工艺流程如下:
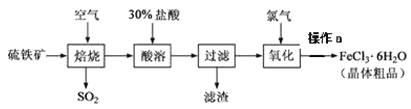
回答下列问题:
(1)在一定条件下,SO2转化为SO3的反应为2SO2+O2![]() 2SO3,该反应的平衡常数表达式为K=____;过量的SO2与NaOH溶液反应的化学方程式为_________________。
2SO3,该反应的平衡常数表达式为K=____;过量的SO2与NaOH溶液反应的化学方程式为_________________。
(2)用36.5%(密度为1.2g·㎝-3)的盐酸的配制500mL的30%(密度为1.095g·㎝-3的盐酸,所需玻璃仪器是 (___)
A.玻璃棒 B.烧杯 C.托盘天平 D.500mL量筒 E、500mL容量瓶 F、胶头滴管
(3)酸溶及后续过程中均需保持盐酸过量,其目的是________________________、
________________________________________________________。
(4)通氯气氧化时,发生的主要反应的离子方程式为_________________________;该过程产生的尾气可用碱溶液吸收,尾气中污染空气的气体为________________(写化学式)。
(5)操作a为_________________________、过滤、洗涤、干燥。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为氢氧燃料电池原理示意图,按照此图的提示,下列叙述不正确的是( )

A.a电极是负极
B.b电极的电极反应为:4OH--4e-====2H2O+O2↑
C.氢氧燃料电池是一种具有应用前景的绿色电源
D.氢氧燃料电池是一种不需要将还原剂和氧化剂全部储藏在电池内的新型发电装置
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用化学原理可以对工厂排放的废水、废渣等进行有效检测与合理处理。某工厂对制革工业污泥中Cr(III)的处理工艺如下:

其中硫酸浸取液中的金属离子主要是Cr3+,其次是Fe3+、Al3+、Ca2+和Mg2+。
(1)酸浸时,为了提高浸取率可采取的措施有___________、__________。
(2)H2O2的作用是将滤液Ⅰ中的Cr3+转化为Cr2O72-,写出此反应的离子方程式:___________。
(3)常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH如下:
阳离子 | Fe3+ | Mg2+ | Al3+ | Cr3+ |
开始沉淀时的pH | 2.7 | —— | —— | —— |
沉淀完全时的pH | 3.7 | 11.1 | 8 | 9(>9溶解) |
加入NaOH溶液使溶液呈碱性,Cr2O72-转化为CrO42-。滤液Ⅱ中阳离子主要有___________;但溶液的pH不能超过8,其理由是_____________________。
(4)钠离子交换树脂的反应原理为:Mn++nNaR→MRn+nNa+,利用钠离子交换树脂除去滤液Ⅱ中的金属阳离子是_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com