
| A. | 35.5g | B. | 71g | C. | 119g | D. | 142g |
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源: 题型:选择题
| X | Y | ||
| Z |
| A. | X与Y可以形成多种化合物 | |
| B. | 简单离子的半径大小:Z<Y<X | |
| C. | X、Y、Z三种元素形成的化合物中既存在共价键又存在离子键 | |
| D. | 在X的最高氧化物对应水化物的浓溶液中加入Z单质,Z不溶解,说明未发生化学反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 同周期元素中,ⅦA族元素的原子半径最大 | |
| B. | ⅥA族元素的原子,其半径越大,越容易得到电子 | |
| C. | 在周期表主族元素的最外层电子数等于其主族序数 | |
| D. | 元素周期表中从ⅢB到ⅡB这10个纵行的元素都是金属元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 聚乙炔是乙炔发生聚合反应形成的高聚物 | |
| B. | 聚乙炔的化学式为 | |
| C. | 聚乙炔是一种碳原子之间以单双键交替结合的链状结构的物质 | |
| D. | 聚乙炔不可能发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
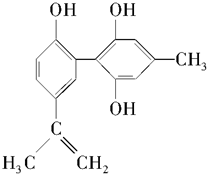
| A. | 遇FeCl3溶液显紫色,因为该物质与苯酚属于同系物 | |
| B. | 该分子中不可能所有碳原子共平面 | |
| C. | 该物质能与浓溴水发生加成反应和取代反应 | |
| D. | 1 mol该物质在催化剂作用下最多能与7 molH2发生加成反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碘单质 | B. | 碘原子 | C. | 碘元素 | D. | 碘离子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com