
【题目】碳酸氢钠用途广泛。可广泛应用于医疗、生活、生产中。回答下列问题:
(1)碳酸氢钠能中和胃酸,碳酸氢钠属于____________(填“酸”“碱”“盐”)
(2)碳酸氢钠能与酒石酸配制固体清凉饮料的发泡剂。将发泡剂溶于水发生反应的离子是_________________。
(3)生活中可用碳酸氢钠蒸馒头,用化学方程式解释其原理__________。将碳酸氢钠加入面团中,若理论上生成二氧化碳0.1mol,需要碳酸氢钠的质量是_______克。
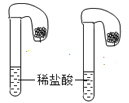
(4)碳酸钠和碳酸氢钠是厨房中常见用品,为鉴别它们,取等质量的样品分别加入如图所示装置的气囊中做对比实验,依据_____________现象,推断哪种样品为碳酸氢钠;写出该反应的离子方程式__________________。
【答案】盐 HCO3-+H+=CO2↑+H2O 2NaHCO3![]() Na2CO3+CO2↑+H2O 16.8 气囊体积大小 HCO3-+H+=CO2↑+H2O、CO32-+2H+=CO2↑+H2O
Na2CO3+CO2↑+H2O 16.8 气囊体积大小 HCO3-+H+=CO2↑+H2O、CO32-+2H+=CO2↑+H2O
【解析】
(1)碳酸氢钠属于盐类;
(2)碳酸氢钠与酸反应产生CO2、H2O;
(3)用碳酸氢钠蒸馒头,涉及碳酸氢钠的分解反应;
(4)等质量时,碳酸氢钠生成的二氧化碳较多,气囊体积较大。
(1)碳酸氢钠电离,生成的阳离子为钠离子,阴离子为酸根离子,属于酸式盐,是盐类;
(2)涉及碳酸氢钠与酸的反应,离子方程式为HCO3-+H+=CO2↑+H2O;
(3)用碳酸氢钠蒸馒头,涉及碳酸氢钠的分解反应,方程式为2NaHCO3![]() Na2CO3+CO2↑+H2O,根据方程式可知生成CO20.1mol,需要0.2molNaHCO3,其质量m(NaHCO3)=0.2mol×84g/mol=16.8g;
Na2CO3+CO2↑+H2O,根据方程式可知生成CO20.1mol,需要0.2molNaHCO3,其质量m(NaHCO3)=0.2mol×84g/mol=16.8g;
(4)等质量时,碳酸氢钠生成的CO2较多,气囊体积较大,涉及反应的离子方程式为HCO3-+H+=CO2↑+H2O、CO32-+2H+=CO2↑+H2O。


科目:高中化学 来源: 题型:
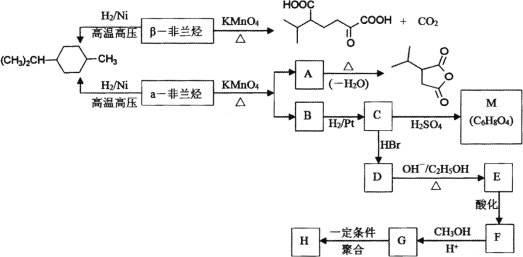
【题目】薄荷油中含有少量的α非兰烃和β非兰烃,两者互为同分异构体,其相对分子质量为136。根据如下转化,回答相关问题:
已知:
![]()
![]()
![]() +RCHO
+RCHO
![]()
![]()
![]() +CO2
+CO2
2CH3COOH![]()
![]()
(1) 写出α非兰烃中官能团名称________,β非兰烃的结构简式________。
(2) 下列有关说法正确的是________。
A.α非兰烃与等物质的量的Br2进行加成反应,产物共有3种
B.C→D和E→F反应类型相同
C.聚合物H易溶于水
D.C→M反应过程中有高分子聚合物等副产物产生
(3) 写出F→G的化学方程式________。
(4) 写出符合下列条件的A的同分异构体________。
①含有4个-CH3;②1 mol此同分异构体在碱性条件下水解需2 mol NaOH。
(5) 以甲苯和丙烯为基本原料合成![]() (用流程图表示,其他无机试剂任选)________。
(用流程图表示,其他无机试剂任选)________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】碳酸钠和碳酸氢钠广泛的应用于我们的生产和生活中。请回答下列问题。
(1)NaHCO3是膨松剂必不可少的成分,受热时能使面胚在焙烧过程中变得松软、多孔。写出受热时NaHCO3发生反应的化学方程式___。
(2)请根据厨房中的物质,设计一实验鉴别某白色粉末是食盐还是食用碱(主要成分为Na2CO3)___。
(3)如图是某兴趣学习小组设计的验证Na2CO3比NaHCO3热稳定性强的实验装置。

①乙处盛放固体药品的化学式是___;②变浑浊的是___烧杯中的澄清石灰水。
(4)兴趣学习小组为研究膨松剂在加热情况下放出气体的量,即:根据单位质量膨松剂产生CO2气体的量来判定其膨胀效果,设计了以下实验,并按如图装置连接(气密性良好,各装置中试剂均过量)。已知:浓硫酸常用于吸收水蒸气;碱石灰是固体氢氧化钠和氧化钙的混合物。回答下列问题:

①装置A中的作用为___。装置E的作用是___,
②如果去掉装置C,该实验会造成测定结果___(“偏大”、“不变”、“偏小”)
③加热前先通入一段时间的空气,再连接D装置,目的是___;停止加热后,还要继续通入一段时间的空气,这样做的目的是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知某可逆反应m A(g)+n B(g) ![]() p C(g)在密闭容器中进行,下图表示在不同反应时间t时,温度T和压强p与反应物B在混合气体中的体积分数B%的关系曲线,由曲线分析,下列判断正确的是( )
p C(g)在密闭容器中进行,下图表示在不同反应时间t时,温度T和压强p与反应物B在混合气体中的体积分数B%的关系曲线,由曲线分析,下列判断正确的是( )

A.T1<T2 p1>p2 m+n>p 放热反应B.T1>T2 p1<p2 m+n>p 吸热反应
C.T1<T2 p1>p2 m+n<p 放热反应D.T1>T2 p1<p2 m+n<p 吸热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某相对分子质量为40的链状不饱和烃A,能发生如下转化:
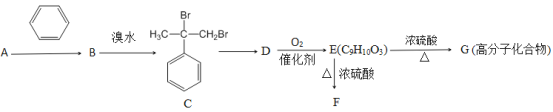
已知:①羟基所连接的碳原子上无氢原子时,难以发生催化氧化;②E能与NaHCO3溶液反应产生气体;③F为酯类化合物。
(1)A的分子式为_____________,A转化为B的反应类型为______________,C转化为D的反应条件为_________________。
(2)B中所含有的官能团的名称为_____________,B中共平面的原子最多有________个。
(3)写出D转化为E的化学方程式:__________________
(4)与E互为同分异构体的芳香族化合物K,已知:①K与E具有相同的官能团;②K不能与FeCl3溶液发生显色反应;③K有二个取代基,则符合上述条件的K共有_________。(填字母代号)
a.3种 b.6种 c. 9种 d.12种
(5)F的结构简式为_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学无处不在,下列说法错误的是( )
A. 《元丰行示德逢》里“雷蟠电掣云滔滔,夜半载雨输亭皋”涉及化学反应:N2+O2 ![]() 2NO
2NO
B. 根据化学学科核心素养之一(证据推理与模型认知)可推知Cr(OH)3胶体也可吸附悬浮杂质
C. 纳米铁粉可以高效地去除污水中的重金属离子是因为其具有较强的还原性
D. 位于贵州省平塘县的中国天眼FAST使用的SiC是一种有机材料
查看答案和解析>>
科目:高中化学 来源: 题型:
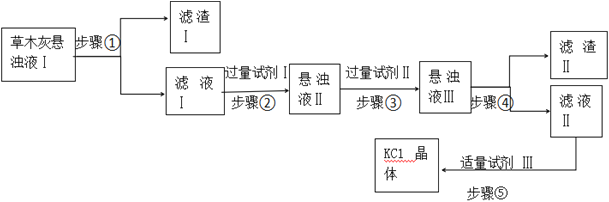
【题目】草木灰主要成分是K2CO3、KCl、K2SO4和不溶于水的杂质。化学实验组为了制取KCl晶体,设计了如下流程。
 回答下列问题:
回答下列问题:
(1)步骤①中用到的玻璃仪器为:烧杯、_____________。
(2)试剂Ⅲ的名称是__________,步骤⑤操作的名称是________。 可供选择的试剂:BaCl2溶液、Ba(NO3)2溶液、K2CO3溶液、Na2CO3溶液、盐酸。步骤②选择的试剂Ⅰ是___________,发生反应的离子方程式为______________;步骤③选择的试剂Ⅱ是__________,其作用是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有短周期主族元素X、Y、Z、R、T,R原子的最外层电子数是电子层数的2倍;Y与Z能形成Z2Y、Z2Y2型离子化合物,Y与T同主族。五种元素原子半径与原子序数之间的关系如图所示。下列推断正确的是( )

A. 离子半径:Y<Z
B. 氢化物的沸点:Y<T
C. 最高价氧化物对应水化物的酸性:T<R
D. 由X、Y、Z、R四种元素组成的常见化合物中含有离子键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】芜湖即将成为安徽省第二个拥有轨道交通的城市。芜湖轨道交通(如图)采用单轨系统,当单轨电车开动时,车上裸露的“电刷”沿架空电线滑动,这种运行方式具有便捷、污染小的特点。下列有关说法不正确的一项是

A.“电刷”材料中很有可能含有石墨
B.“电刷”材料一定含有导电性、润滑性极好的材料
C.采用单轨系统提高了能量的利用效率,符合绿色化学的要求
D.单轨列车运行时,供电原理与原电池类似
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com