

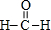 ��XΪNaOH�������ʽΪ��
��XΪNaOH�������ʽΪ�� ��
��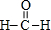 ��
�� ��
��| 0.0056L |
| 22.4L/mol |
| ||
| 10-3mol |
| 0.1L |
| �� |
| �� |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���Ҵ������ᣩ��������̼������Һ��������Һ |
| B�����飨��ϩ�� H2�������� ������ |
| C����ϩ��SO2�� ��ˮ ϴ�� |
| D���������������ᣩ ����̼������Һ ��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���μӼ��ȳʺ�ɫ����Һ��K+��Fe2+��NO3-��Cl- |
| B����ˮ�������c��H+��=10-12mol?L-1����Һ��Na+��K+��ClO-��SO32- |
| C��0.1mol?L-1NH3?H2O��Һ��Cu2+��NH4+��NO3-��SO42- |
| D����ɫ����Һ�壺K+��Na+��C6H5O-��HCO3- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�����³�ѹ�£�36g C5H10������һ������7NA�����õ��Ӷ� |
| B��6g�����������ǵĻ������������������ȫȼ������0.2NA��ˮ���� |
| C��10mL5mol/L ��NH4��2SO4��Һ�к���NH4+��ĿΪ0.1NA�� |
| D��1mol FeCl3���ת��ΪFe��OH��3������γ�NA������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��Al13��Al14��Ϊͬλ�� |
| B��Al13��Al14������ԭ�ӡ���ԭ�Ӽ�ͨ�����Ӽ���� |
| C��All4����ʧȥ2�����Ӷ��γ��ȶ���All42+ |
| D��Al13���н�ǿ�Ļ�ԭ�ԣ�����ʧȥ���Ӷ��γ������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ���ԭ���ڻ�ѧ��ҵ���й㷺��Ӧ�ã���ͼ��ʾһ�����أ�װ�е��Һa��X��Y������缫�壬ͨ��������ֱ����Դ��������ش��������⣺
���ԭ���ڻ�ѧ��ҵ���й㷺��Ӧ�ã���ͼ��ʾһ�����أ�װ�е��Һa��X��Y������缫�壬ͨ��������ֱ����Դ��������ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��FeCl2��Һ��ͨ��Cl2��Fe2++Cl2��Fe3++2Cl- | ||
| B��Ba��OH��2��Һ������ķ�Ӧ OH-+H+�TH2O | ||
| C��Al��OH��3�����еμ����� Al��OH��3+3H+�TAl3++3H2O | ||
D��AlCl3��Һ�м��������ˮ��Al3++4OH-��AlO
|
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com