
| A、Fe与足量的Br2反应可以制得大量的FeBr3,故Fe与足量I2蒸气反应也可以制得大量的FeI3 |
| B、CO2气体通入Ca(ClO)2溶液中可以得到HClO,故SO2气体通入Ca(ClO)2溶液中也一定能得到HClO |
| C、FeCl3溶液加热蒸干后得不到FeCl3,故Fe2(SO4)3溶液加热蒸干后也得不到Fe2(SO4)3 |
| D、Cu(OH)2可溶于HNO3溶液,故Al(OH)3也可溶于HNO3溶液 |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 物质 | Cu(OH)2 | Fe(OH)3 | CuCl | CuI |
| Ksp | 2.2×10-20 | 2.6×10-39 | 1.7×10-7 | 1.3×10-12 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 元素名称 | 氟 | 氧 | 溴 | 碘 | 铍 |
| 第一电离能(kJ/mol) | 1681 | 1251 | 1140 | 1008 | 900 |
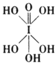 )和HIO4,前者为五元酸,后者为一元酸.请比较二者酸性强弱:H5IO6
)和HIO4,前者为五元酸,后者为一元酸.请比较二者酸性强弱:H5IO6查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
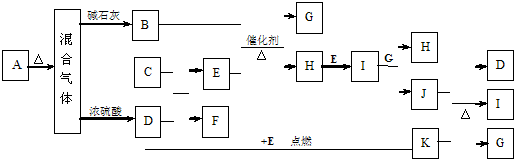
 甲、乙是两种常见的化合物,X、Y、Z是三种常见的单质.下表所列各组物质中,物质之间通过一步反应不能实现如图所示转化的是( )
甲、乙是两种常见的化合物,X、Y、Z是三种常见的单质.下表所列各组物质中,物质之间通过一步反应不能实现如图所示转化的是( )| 选项 | X | Y | Z | 甲 | 乙 |
| A | C | H2 | O2 | H2O | CO |
| B | Zn | Fe | Cl2 | Fe Cl2 | ZnCl2 |
| C | Mg | C | O2 | CO2 | MgO |
| D | H | Si | Cl2 | SiCl4 | HCl |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com