
【题目】将铁屑溶于过量盐酸后,再加入下列物质,不会有Fe 3+的是( )
A. FeCl3溶液 B. 硝酸锌 C. CuSO4 D. H2O2
科目:高中化学 来源: 题型:
【题目】生产生活中广泛涉及氧化还原反应
Ⅰ.研究电化学腐蚀及防护的装置如图所示
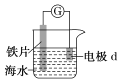
(1)若d为石墨,石墨上的电极反应式为_________________ ;
(2)若d为锌,锌上的电极反应式为___________________;
(3)将图中电流表换成外接电源,铁片接___________(填“正”或“负”)极被保护
Ⅱ.高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,比Cl2、O2、ClO2、KMnO4氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
(1)干法制备高铁酸钾的主要反应为:2FeSO4+ 6Na2O2![]() 2Na2FeO4+2Na2O+2Na2SO4+O2↑
2Na2FeO4+2Na2O+2Na2SO4+O2↑
①该反应中的氧化剂是________________,还原剂是_______________,每生成1 molNa2FeO4转移_______mol电子。
②简要说明K2FeO4作为水处理剂时所起的作用_________________________________
(2)湿法制备高铁酸钾(K2FeO4)的反应体系中有六种粒子:Fe(OH)3、ClO-、OH-、FeO42-、Cl-、H2O。
①写出并配平湿法制高铁酸钾反应的离子方程式:____________________________。
②每生成1 mol FeO42-转移________mol电子,若反应过程中转移了0.3 mol电子,则还原产物的物质的量为________mol。
③低温下,在高铁酸钠溶液中加入KOH至饱和可析出高铁酸钾(K2FeO4),说明什么问题______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Z、Q、R、T、U分别代表原子序数依次增大的短周期元素,周期表的全部元素中X的原子半径最小,X与R的最外层电子数相等;Z的内层电子数是最外层电子数的一半,U的最高化合价和最低化合物的代数和为6;R和Q可形原子数之比为1:1和2:1的两种化合物;R、T、U三者的最高价氧化物对应的水化物两两之间能发生化学反应.请回答下列问题:
(1)T元素在期表中的位置是________;由上述元素中的四种元素形成的既含有离子键又含有共价键的化合物为________(写出其中一种物质的名称).
(2)X、Z、Q三种元素的原子半径由小到大顺序为________(填元素符号).
(3)T、U两元素最高价氧化物对应的水化物反应的离子方程式为________.
(4)下列可以判断R和T金属性强弱的是________(填序号).
a.单质的熔点R比T低 b.单质与酸反应时,失电子数R比T少
c.单质与水反应R比T剧烈 d.最高价氧化物的水化物的碱性R比T强
(5)某同学用Q、R两元素的单质反应生成固体物质R2Q2,R2Q2属于离子化合物,且能与化合物X2Q反应生成Q的单质.R2Q2的电子式为________;R2Q2与X2Q反应的化学方程式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种新型的电池,总反应为: 3Zn+2FeO42-+8H2O=2Fe(OH)3↓+3Zn(OH)2↓+4OH—,其工作原理如图所示。下列说法不正确的是
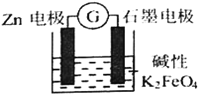
A. Zn极是负极,发生氧化反应
B. 随着反应的进行,溶液的pH增大
C. 电子由Zn极流出到石墨电极,再经过溶液回到Zn极,形成回路
D. 石墨电极上发生的反应为:FeO42—+3e—+4H2O=Fe(OH)3↓+5OH—
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】白磷与氧可发生如下反应:P4+5O2=P4O10。已知断裂下列化学键需要吸收的能量分别为:P—P akJ·mol—1、P—O bkJ·mol—1、P="O" ckJ·mol—1、O="O " dkJ·mol—1。

根据图示的分子结构和有关数据估算该反应的△H,其中正确的是( )
A. (6a+5d-4c-12b)kJ·mol—1B(4c+12b-6a-5d)kJ·mol—1 B. (4c+12b-4a-5d)kJ·mol—1
C. (4a+5d-4c-12b)kJ·mol—1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图中烧杯里盛的是天然水,铁被腐蚀由快到慢的顺序是( )
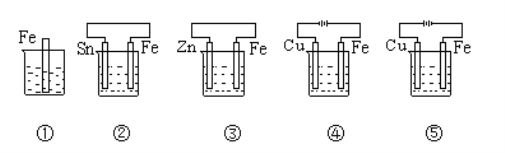
铁被腐蚀由快到慢的顺序是
A. ③〉②〉①〉④〉⑤ B. ④〉②〉①〉③〉⑤
C. ③〉②〉④〉⑤〉① D. ④〉⑤〉②〉③〉①
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】全固态锂硫电池能量密度高、成本低,其工作原理如图所示,其中电极 a常用掺有石墨烯的S8材料,电池反应为:16Li+xS8=8Li2Sx(2≤x≤8)。下列说法错误的是( )

A. 电池工作时,正极可发生反应:2Li2S6+2Li++2e-=3Li2S4
B. 电池工作时,外电路中流过 0.02 mol 电子,负极材料减重 0.14 g
C. 石墨烯的作用主要是提高电极a的导电性
D. 电池充电时间越长,电池中Li2S2的量越多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“生物质能”主要是指树木、庄稼、草类等植物直接或间接提供的能量,下列说法不正确的是
A. 生物质能是可储存和可运输的非可再生能源 B. 生物质能和化石燃料一样属于一次能源
C. 生物质能是解决农村能源的主要途径 D. 利用生物质能就是间接利用太阳能
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com