
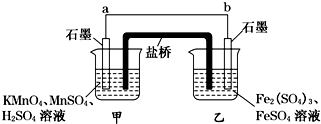


科目:高中化学 来源: 题型:
| A、苯硝化,苯酚和溴水反应,皂化反应,乙烯与溴水反应 |
| B、酯的水解,酯化反应,乙醇和氢卤酸反应,乙醇和浓硫酸加热至140℃时的反应 |
| C、淀粉在硫酸存在下制葡萄糖,醛的氧化或还原 |
| D、纤维素水解,浓硫酸和乙醇在170℃时的反应,蛋白质水解 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、10.00ml |
| B、15.00ml |
| C、大于15.00ml |
| D、小于15.00ml |
查看答案和解析>>
科目:高中化学 来源: 题型:
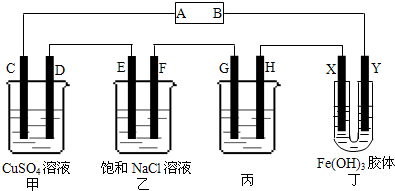
查看答案和解析>>
科目:高中化学 来源: 题型:
| NaCN |
| H2O |
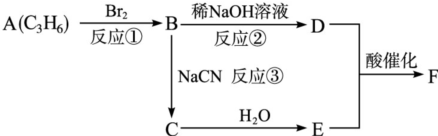
查看答案和解析>>
科目:高中化学 来源: 题型:
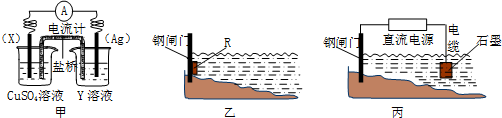
| ||
| 充电 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、升高温度,Kw增加,pH增大 |
| B、向水中加入少量NaOH固体,平衡向逆方向移动,c(OH-)增大 |
| C、向水中加入少量CH3COONa固体,平衡向正方向移动,c(H+)增大 |
| D、25℃时,纯水中c(H+)>10-7mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
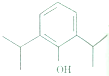 2009年8月25日洛杉矶首席验尸官在休斯顿法庭上公布流行音乐天王杰克逊被注射异丙酚,“天王星”就此陨落.异丙酚是一种强力的镇静剂,常被麻痹医生称为“牛奶”.其结构如图所示,下列有关异丙酚的说法不正确的是( )
2009年8月25日洛杉矶首席验尸官在休斯顿法庭上公布流行音乐天王杰克逊被注射异丙酚,“天王星”就此陨落.异丙酚是一种强力的镇静剂,常被麻痹医生称为“牛奶”.其结构如图所示,下列有关异丙酚的说法不正确的是( )| A、能发生加成反应 |
| B、能和FeCl3溶液发生显色反应 |
| C、能与Na2CO3溶液发生反应 |
| D、分子中所有碳原子都在同一平面上 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、含2NA个氢分子的氢气 |
| B、17g氨气(NH3的摩尔质量为17g?mol-l) |
| C、0.8mol氧气 |
| D、标准状况下11.2 L氯气 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com